
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
苯环上有两个取代基的C9H12,其一氯代物的同分异构体共有(不考虑立体异构) ( )
A.10种 B.14种 C.19种 D.26种
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列说法错误的是 ( )
A.分子组成为C4H100的醇有4种
B.1 mol二氯乙烷与Cl2发生取代反应,反应完全共需4 mol Cl2
C.(CH3)3CCH2CH3的一氯代物有3种
D.乙烷与Cl2反应与乙烯与C12的反应类型相同
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
已知谷胱甘肽水解后产生的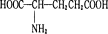 同分异构体有很多,其中含有一个甲基、一个硝基和一个羧基的同分异构体共有 ( )
同分异构体有很多,其中含有一个甲基、一个硝基和一个羧基的同分异构体共有 ( )
A.4种 B.5种 C.6种 D.7种
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列各项中,用来表示物质的组成或结构的模型是 ( )
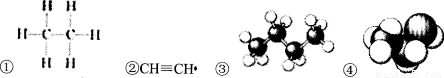
A.①②③④ B.①和② C.③和④ D.只有①
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.乙醇分子中的氢原子均可被金属钠置换
B.烃分子中的氢原子被羟基取代后的衍生物都属于醇
C.甲醇是最简单的醇,它不能发生消去反应生成烯烃
D.某一元醇在浓硫酸存在下加热到170℃可以生成丙烯,该一元醇一定是1-丙醇
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
香叶醇是合成玫瑰香油的主要原料,其结构简式如图所示。下列有关香叶醇的叙述正确的是 ( )
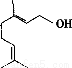
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1。 请回答下列问题:
(1)这四种元素中电负性最大的是 (填元素符号)、第一电离能最小的是 (填元素符号);
(2)C所在的主族元素气态氢化物中,沸点最低的是 (填化学式);
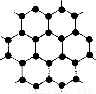
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为 ;
(4)D的醋酸盐晶体局部结构如右图,该晶体中含有的化学键是 (填选项序号);
①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如下图:

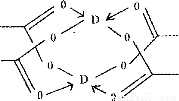
第①步产生的棕色的烟属于 (填一种分散系),如第②步加大量水,溶液呈 色,
写出第⑤步反应的离子方程式: 。
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为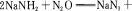

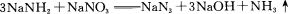 回答下列问题:
回答下列问题:
(1)氮所在的周期中,电负性最大的元素是 ,第一电离能最小的元素是 。
(2)基态氮原子的L层电子排布图为 。
(3)与N3-互为等电子体的分子为 (写出一种)。依据价层电子对互斥理论,NO3-的空间构型为 。
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)的晶体类型为 。叠氮化钠的水溶液呈碱性,用离子方程式表示其原因: 。
(5)N20沸点(一88.49℃比NH3沸点(一33.34℃)低,其主要原因是
(6)安全气囊的设计原理为
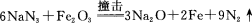
①氮分子中δ键和π键数目之比为 。
②铁晶体中存在的化学键类型为 。
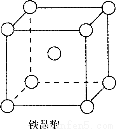
③铁晶体为体心立方堆积,其晶胞如图所示,晶胞边长为a cm,该铁晶体密度为
(用含a、NA的表达式表示,其中NA为阿伏加德罗常数)。
查看答案和解析>>
科目: 来源:2013-2014黑龙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数。R是由A、D两元素形成的离子化合物,其中A+与D2一离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体内晶体类型应属于 (填写“六方”、“面心立方”或“体心立方”)堆积,空间利用率为 。
(2)C3-的电子排布式为 ,在CB3分子中C元素原子的原子轨道发生的是 杂化,CB3分子的VSEPR模型为 。
(3)C的氢化物在水中的溶解度如何 ,为什么具有这样的溶解性 。
(4)D元素与同周期相邻元素的第一电离能由大到小的关系是:
(用元素符号表示);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱: 。
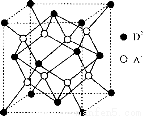
(5)如图所示是R形成的晶体的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是p g·cm-3试计算R晶体中A+和D2-最短的距离 。
(阿伏加德罗常数用NA表示,只写出计算式,不用计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com