
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)下列离子方程式错误的是
A.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O
B.向KI溶液中加H2SO4溶液后振摇:4H+ + 4I-+ O2 = 2I2 + 2H2O
C.酸性高锰酸钾中加入草酸,溶液褪色:2MnO4- + 5H2C2O4 + 6 H+ = 2Mn2+ + 10CO2↑ +8H2O
D.证明C的非金属性强于Si的反应:SiO32- + CO2+ H2O = H2SiO3↓+ CO32-
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)下图表示500℃时,X、Y、Z三种气体在容积固定的容器中反应,各物质的浓度随时间的变化情况。达到平衡后,改变压强,平衡不移动。下列说法中正确的是
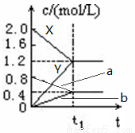
A.Z物质的变化情况为曲线b
B.该反应的化学方程式为:2X(g) 3Y(g) + Z(g)
3Y(g) + Z(g)
C.0→t1,X的物质的量浓度变化量为1.2mol/L
D.若t1= 1min,则v(Y )= 0.02 mol·L-1·s-1
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)某课外研究小组的同学将FeCl3(aq)滴加到5%H2O2溶液后,发现产生无色气体由慢到快,最后再变慢;溶液温度升高;同时溶液颜色由黄色立即变为棕褐色,当反应殆尽时,溶液又恢复黄色,由此得出以下结论,你认为错误的是
A.H2O2的分解反应为放热反应
B.FeCl3是H2O2分解反应的催化剂
C.与不加FeCl3(aq)相比,当H2O2均完全分解时,加FeCl3(aq)使反应放出的热量更多
D.若将少量FeCl2溶液滴入过量5%H2O2溶液中,则除溶液颜色变化不同外,其它现象相同
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)已知:HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是
A.对比等浓度的两种酸的pH
B.对比等浓度的两种酸,与相同大小镁条反应的初始速率
C.对比等浓度、等体积的两种酸,与等量NaOH溶液反应后放出的热量
D.对比等浓度、等体积的两种酸,与足量Zn反应,生成H2的体积
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
电镀废液中Cr2O72-可通过下列反应转化成铬黄(PbCrO4):
Cr2O72-(aq)+ 2Pb2+(aq)+ H2O(l) 2PbCrO4(s)+ 2H+(aq)△H<0
2PbCrO4(s)+ 2H+(aq)△H<0
该反应达平衡后,改变条件,下列说法正确的是
A.移走部分PbCrO4固体,Cr2O72-转化率升高
B.升高温度,该反应的平衡常数(K)增大
C.加入少量NaOH固体,自然沉降后,溶液颜色变浅
D.加入少量K2Cr2O7固体后,溶液中c(H+)不变
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)科学家发现海洋是一个名副其实的“聚宝盆”,一些国家觊觎我国南海海域的丰富资源,导致近年来南海争端不断。下列对海洋资源开发利用的说法不正确的是
A.海底如“土豆”般的金属结核矿含有铁、锰、钴等多种元素,可用铝热法冶炼并分离得到各种金属单质
B.海水淡化工厂可与化工生产结合,如淡化后的浓海水,可用于提溴、镁、钠等
C.海水中的金、铀等元素储量高、浓度低,提炼时,须先富集
D.海水提镁过程中,所需的石灰乳,可用贝壳煅烧后加水得到,体现了就地取材、降低成本的生产理念
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
已知有反应:I2(g)+H2(g) 2HI(g)△H<0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
2HI(g)△H<0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
选项 | X | Y |
|
A | 温度 | 容器内混合气体的密度 | |
B | I2的物质的量 | H2的转化率 | |
C | H2的浓度 | 平衡常数K | |
D | 加入Ar的物质的量 | 逆反应速率 |
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)向100mL 0.1mol/L醋酸溶液中加入下列物质,混合溶液有关量或性质变化趋势正确的是
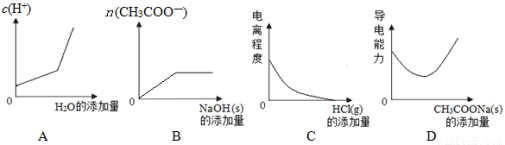
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
已知2SO2 (g)+O2 (g)  2SO3 (g);△H =﹣197kJ?mol﹣1,向同温、同体积的三个密闭容器中分别充入气体,起始投料量如下表:
2SO3 (g);△H =﹣197kJ?mol﹣1,向同温、同体积的三个密闭容器中分别充入气体,起始投料量如下表:
| SO2 (mol) | O2 (mol) | SO3 (mol) |
甲 | 2 | 1 | 0 |
乙 | 4 | 2 | 0 |
丙 | 0 | 0 | 2 |
恒温、恒容下反应达平衡时,下列关系一定正确的是
A.SO3的质量m:2m甲 = m乙
B.容器内压强P:2P丙 > P乙
C.反应放出或吸收热量的数值Q:Q甲 > Q丙
D.c(SO2)与c(O2)之比a:a丙 > a乙
查看答案和解析>>
科目: 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:填空题
(12 分)T℃时,在某容积恒为2L密闭容器中充入2molN2、4molH2,在催化剂辅助下发生反应:N2(g)+3H2(g) 2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。
2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。
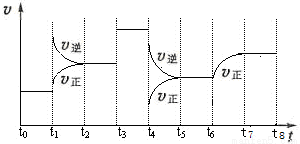
试回答下列问题:
(1)T℃时,N2的转化率为:___________,该反应的平衡常数K=___________。
(2)T℃时,下列能证明该反应已经建立平衡状态的是:__________________。
A.体系总压强不再改变
B.混合气体颜色不再改变
C.H2的质量百分含量不再改变
D.c(N2)与c(NH3)的比值不再改变
(3)t1时刻,改变的外界条件是__________,平衡常数K(t5~t6) ______ K(t7~t8)(填“>、<或=”,下同)。
(4)T℃时,建立平衡后,向容器中加入2molN2和2molNH3,则此时 v正 ___ v逆。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com