
科目: 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:填空题
(1)NaClO溶液在碱性条件下将CN-氧化成无毒的碳酸根离子和N2,该反应离子方程式 。
(2)A、B、C、D四种元素,它们的原子序数依次增大,且均小于18,A和B在同一周期,A原子p能级有一个空轨道,B原子的p能级有两个未成对电子,0.1mol C单质能从酸中置换出 2.24L氢气(标准状态),此时它就变成与B离子电子层排布完全相同的离子。D离子的半径在B、C、D中为最小。则:
①A是_________,B是_________,C是_________,D是_______。(填名称)
②A单质和B单质充分反应生成的化合物的结构式是____________。
③B的一种同位素形成的单质,1mol这种单质中含中子的物质的量是20mol,则这种同位素原子质量数________。
(3)NH3·H2O的电离方程式为NH3·H2O NH4++OH-,试判断溶于水后,形成的合理结构是________。(填右图中的字母)
NH4++OH-,试判断溶于水后,形成的合理结构是________。(填右图中的字母)
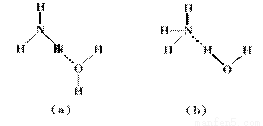
(4)把CoCl2溶于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+,此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示,Co的配位数是6。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1molCoCl3·5NH3只生成2molAgCl,CoCl3·5NH3中Co化合价为 ,请写出表示此配合物结构的化学式: 。
(5)H2O、H2S、H2Se熔沸点由低到高的顺序: 。
(6)HF比HCl热稳定 (填“强”或“弱”),原因是: ____________ 。
查看答案和解析>>
科目: 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:填空题
铜是过渡金属元素,可以形成多种化合物。
(1)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O
①电负性:C ______O(填“>”或“=”或“<”)。
②CO常温下为气体,固态时属于 晶体。
(2)Cu+与NH3形成的配合物可表示成[Cu(NH3)n]+,该配合物中,Cu+的4s轨道及4p通过sp杂化接受NH3提供的电子对。
[Cu(NH3)n]+ 中Cu+ 与n个氮原子的空间结构呈 型,n= 。
(3)CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
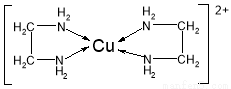
请回答下列问题:
①配离子[Cu(En)2]2+的中心原子基态第L层电子排布式为 。
②乙二胺分子中氮原子轨道的杂化类型为 ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是: 。
③配合物[Cu(En)2]Cl2中不存在的作用力类型有 (填字母);
A 配位键 B 极性键 C 离子键 D 非极性键 E.氢键 F.金属键
查看答案和解析>>
科目: 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:填空题
1-36号A、B、C、D、E 、F六种元素,其中A、B、C、D、E的原子序数均小于18且其核电荷数依次递增,B元素基态原子电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,D原子的价电子排布为ns2np2n+2, E原子第一至第四电离能(kJ·mol-1)分别为:738、1451、7733、10540。F2+离子K、L、M层全充满。根据以上信息,同答下列问题:
(1)BA4D和BA2D,沸点较高的是 (填相关物质的结构简式)
(2)已知B与A形成的化合物在标准状况下的密度为1.16g·L-1,则在该化合物分子空间构型 ,在该化合物分子中含有σ键和π键个数比 。
(3)写出单质F与足量C的最高价氧化物对应的水化物稀溶液反应,C被还原到最低价,该反应的化学方程式 。
(4)下图能正确表示第三周期部分元素的第二电离能(I2)与原子序数关系 (填标号)。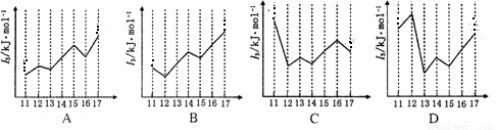
(5)B的单质是一种层状结构,元素B和E的形成一种合金,E的原子位于B的层间,其投影位于层面六圆环的中央,“△”表示E的原子位置,平行四边形表示在此二维图形上画出的一个晶胞,该合金的化学式为________。
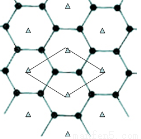
查看答案和解析>>
科目: 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
在25℃、1×105Pa时,等质量的H2、Cl2、CO2、C2H2四种气体中( )
A. H2分子数最大 B. C2H2原子数最大
C. CO2密度最大 D. Cl2分子间平均距离最大
查看答案和解析>>
科目: 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
基于实验现象的推论,你认为合理的是( )
选项 | 实验现象 | 推论 |
A | 乙烯气体可以使溴水褪色 | 乙烯发生取代反应 |
B | 浓硫酸电导率比较低 | 硫酸浓度大时是弱电解质 |
C | 氨气用于喷泉实验 | 氨气极易溶于水 |
D | 硝酸溶液使pH试纸先变红后变白 | 硝酸酸性太强不能用pH试纸检测 |
查看答案和解析>>
科目: 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
对于相应化学用语的推论合理的是( )
选项 | 化学用语 | 推论 |
A |
| 该铀离子核外有89个电子 |
B | 2H2(g)+O2(g)= 2H2O(g);△H=-483.6kJ?mol | 1mol氢气完全燃烧放出热量483.6kJ. |
C | 2NaCl+2H2O | NaCl氧化性比Cl2强 |
D | FeO+4H++NO3―= Fe3++NO2↑+2H2O | 氧化亚铁溶于稀硝酸的离子方程式 |
查看答案和解析>>
科目: 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),下列说法正确的是 ( )
2Z(g),下列说法正确的是 ( )
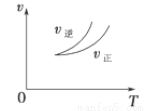
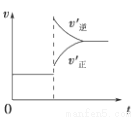
A.左上图说明正反应为吸热反应
B.反应达平衡后,增大压强气体密度将减小
C.右上图可表示升高温度使平衡向逆反应方向移动
D.右上图虚线可表示使用催化剂后引发的反应速率变化
查看答案和解析>>
科目: 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用。某型甲醇燃料电池的总反应式2CH4O + 3O2 = 2CO2↑+ 4H2O,下图是该燃料电池的示意图。下列说法错误的是( )
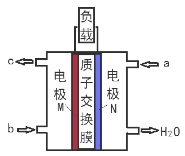
A.燃料电池将化学能转化为电能
B. a是甲醇、b是氧气
C.质子从M电极区穿过交换膜移向N电极区
D.负极反应:CH4O - 6e- + H2O = CO2↑+ 6H+
查看答案和解析>>
科目: 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
常温下,向l00mL 0.01 mol?L-1 盐酸中逐滴加入0.02 mol?L-1 MOH溶液,如下图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是( )
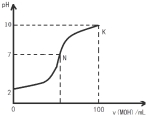
A.MOH是弱碱
B.N点c(Cl-) = c(M+)
C.随着MOH溶液的滴加,比值 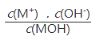 不变
不变
D.K点对应的溶液c(MOH)+c(OH-)-c(H+) = 0.005 mol?L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com