
科目: 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
已知:
(1)胆矾失水的热化学方程式为CuSO4·5H2O(s)===CuSO4(s)+5H2O(l) ΔH=+Q1 kJ/mol
(2)室温下,无水硫酸铜溶于水的热化学方程式为CuSO4(s)===Cu2+(aq)+SO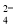 (aq) ΔH=
(aq) ΔH=
-Q2 kJ/mol
(3)胆矾(CuSO4·5H2O)溶于水时溶液温度降低。则Q1与Q2的关系是(Q1、Q2为正数) ( )
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法确定
查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列关于实验的描述错误的一项是 ( )
A.取5mL 0.1 mol/L KI溶液,滴加0.1mol/LFeCl3溶液5~6滴,继续加入2 mLCCl4,充分振荡,取上层溶液,滴加KSCN溶液,溶液呈现血红色,证明溶液中还存在Fe3+
B.在铁钉的析氢腐蚀实验中,在负极周围加入K3[Fe(CN)6]溶液会出现蓝色沉淀
C.燃料电池实验中,用KNO3溶液或Na2SO4溶液代替蒸馏水,效果要好得多
D.蔗糖的“黑面包”实验中只体现了浓硫酸的脱水性
查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:填空题
按要求填空:
(1)原子种类由 决定;第三周期半径最小的元素形成的简单离子的离子结构示意图是 ;
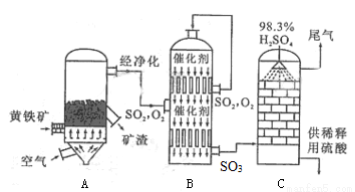
(2)以黄铁矿为原料生产硫酸的工艺流程如下左图所示,设备B的名称为 ;设备A中发生反应的化学方程式 ;
(3)如下右图是实验室中常用于测定盐酸和氢氧化钠溶液反应热的装置,此装置名称叫 ;
(4)0.5 mol CH3OH(l)完全燃烧生成二氧化碳气体和液态水时放出热量为363.2 kJ,写出表示CH3OH(l)燃烧热的热化学方程式 。

查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:填空题
工业上电解制碱的技术是用阳离子交换膜法,主要原料是饱和食盐水。下图为阳离子交换膜法电解原理示意图:
请回答下列问题:
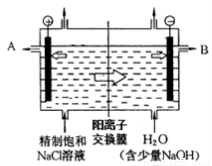
(1)A极为电解槽的________极,B极的材料工业上常采用的是生活中常见的金属,但有大量损耗,其主要原因是 。(填“吸氧腐蚀”或“析氢腐蚀”)
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号)。
①H2,②Cl2,③H+,④Cl-,⑤Na+,⑥OH-。
(3)若上述电解过程中用阴离子交换膜代替阳离子交换膜(已知:3Cl2 +6OH-==5Cl-+ClO3-+3H2O),下列说法正确的组合是 。
A.电解结束时,右侧溶液中含有ClO3—
B.电解槽内发生反应的总化学方程式为:NaCl + 3H2O  NaClO3 + 3H2↑
NaClO3 + 3H2↑
C.用阴离子交换膜后,电解槽内两个电极发生的电极反应与原来一样
D.用阴离子交换膜后,阳离子的定向移动方向与原来相反
(4)已知某电解槽每小时加入10%的氢氧化钠溶液a kg,每小时能产生标准状况下的氯气b L,则电解后流出的氢氧化钠溶液(密度为d g·cm-3)的物质的量浓度为(理论计算,需化简) mol/L。
查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:填空题
催化剂是化工技术的核心,绝大多数的化工生产均需采用催化工艺。
(1)人们常用催化剂来选择反应进行的方向。下左图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
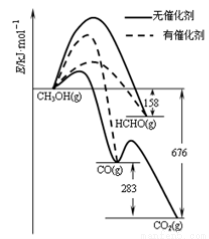
①在有催化剂作用下,CH3OH与O2 反应主要生成 (填“CO、CO2、HCHO”);
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g) △H= 。
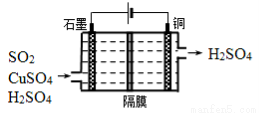
(2)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2n Cu+(n+1)O2+(2-2 n) H2O=2n CuSO4+(2-2n) H2SO4
从环境保护的角度看,催化脱硫的意义为 ;每吸收标准状况下11.2L SO2,被SO2还原的O2的质量为 g。
②利用下图所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式 。
查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:填空题
化合物A由N、H两种元素组成,0.01mol A与足量CuO充分反应生成红色Cu的同时,生成了0.36g水和标准状况下的体积为0.224L的N2。B是由Na和H两元素组成的离子化合物,能与水反应生成H2,称为产氢剂。化合物C的焰色反应为黄色,根据质谱分析它的相对分子质量为39且与水反应能生成氨气。
(1)A的化学式为 ;A与CuO反应的化学方程式为 。
(2)B的电子式为 。
(3)C中存在的化学键 ;C与过量稀盐酸反应的化学方程式为 。
(4)有一种理想的化合物NH4H,经查阅资料,该物质至今未能制得,请说明可能的原因
。
查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:填空题
Cu(NO3)2是重要的化工原料。回答下列工业生产和化学实验中的几个问题。
(1)实验室欲制备0.3 mol Cu (NO3)2晶体,甲、乙两同学分别设计实验方案如下:
甲:Cu  Cu(NO3)2 乙:Cu
Cu(NO3)2 乙:Cu 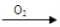 CuO
CuO  Cu(NO3)2
Cu(NO3)2
①从绿色化学的角度分析, 同学的方案更合理,此同学可节约2mol/L的稀硝酸 mL;
②乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择
方案(填字母序号)。
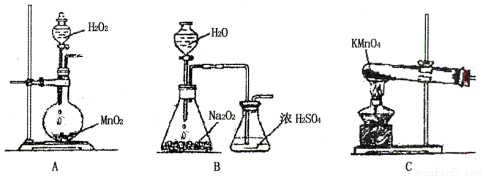
③有下述装置(如下图),当装置电路中通过2mol电子时,Cu电极(填编号) 。
(a)增重64g (b)减重64g (c)可能增重64g,也可能减重64g
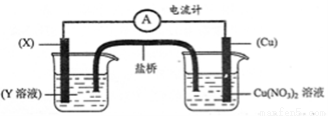
(2)①某校化学兴趣小组的同学对硝酸铜的受热分解进行探究。他们设计了如下图装置加热Cu(NO3)2固体(加热及夹持装置未画出)。加热过程发现:装置①中的固体逐渐变为黑色;装置②中有气泡产生,但在上升的过程中消失;石蕊试液逐渐变为红色,液体几乎不被压至装置③中。请写出Cu(NO3)2受热分解的化学方程式: ;
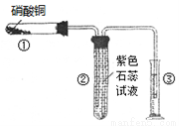
②在装置中①试管的橡皮塞最好用锡箔包住,原因是 。
(3)NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为 。

查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:选择题
“化学无处不在”,下列与化学有关的说法正确的是 ( )
A.聚乙烯塑料的老化是因为发生了加成反应
B.纤维素在人体内可水解为葡萄糖,故可作人类的营养物质]
C.合成纤维、人造纤维及碳纤维都属于有机高分子材料
D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现紫蓝色,则该溶液含有氨基酸
查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:选择题
“化学是人类进步的关键”。下列说法不正确的是 ( )
A.PM2.5是指空气中直径≤2.5 μm的固体颗粒或液滴的总称
B.根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间
C.科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通DNA链中的P元素
D. 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物 ,该反应符合绿色化学的原则
,该反应符合绿色化学的原则
查看答案和解析>>
科目: 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法一定正确的是 ( )
A.常温下,1 L 0.1 mol/L的NH4NO3溶液中氧原子数为0.3NA
B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA
C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的O原子数目为0.2NA
D.Fe与水蒸气在高温条件下反应,有1 mol Fe参与反应,则转移电子的数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com