
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:选择题
如图装置,U形管中装有50 mL 2 mol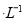 的CuSO4溶液。通电一段时间后,下列说法正确的是
的CuSO4溶液。通电一段时间后,下列说法正确的是
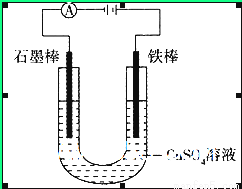
A.转移0.2 mol电子时,阳极减少质量大于阴极增加质量
B.转移0.4 mol电子时,阴极得到2.24 L标准状况下的气体
C.电解一段时间后,U形管中会产生红褐色物质,后来逐渐溶解
D.若将石墨棒换成铜棒,可实现铁制品上镀铜
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:选择题
T℃时,CaCO3和CaF2的Ksp分别为1.0 ×10-10。和4.0 ×10-12。下列说法正确的是
A.T℃时,两饱和溶液中c(Ca2+ ):CaCO3>CaF2
B.T℃时,两饱和溶液等体积混合,会析出CaF2固体
C.T℃时,CaF2固体在稀盐酸中的Ksp比在纯水中的Ksp大
D.T℃时,向CaCO3悬浊液中加NaF固体,可能析出CaF2固体
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:选择题
分子式为C9H12O,苯环上有两个取代基且含羟基的化合物,其可能的结构有
A.9种 B.12种 C.15种 D.16种
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
(14分)常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。
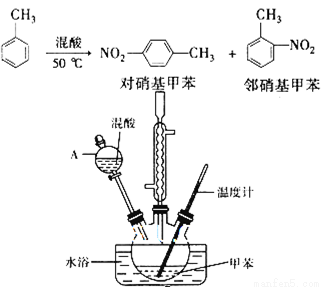
实验中可能用到的数据:
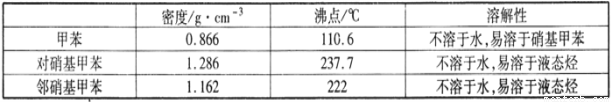
实验步骤:①按体积比1:3配制浓硫酸与浓硝酸混合物40 mL;
②在三颈瓶中加入15 mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60 g。
请回答下列问题:
(1)配制混酸的方法是________。反应中需不断搅拌,目的是____________________
_____________________________。
(2)仪器A的名称是________ ,使用该仪器前必须进行的操作是_________。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是_________。
(4)分离反应后产物的方案如下:

其中,操作1的名称为________,操作2中需要使用下列仪器中的________(填序号)。
A.冷凝管 B.酒精灯 C.温度计 D.分液漏斗 e.蒸发皿
(5)该实验中一硝基甲苯的产率为________(保留两位有效数字)。
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
(14分)工业上可用软锰矿浆(主要成分为MnO2)吸收硫酸厂废气SO2,并制备MnSO4.H2O晶体,其工艺流程如下:

已知:①浸出液的pH<2,且阳离子主要是Mn2+,以及少量Fe2+、Al3+等。
②几种离子沉淀时数据信息如下:

请回答下列问题:
(1)浸出液pH <2的原因可能是_________________________________________。
(2)加入MnO2,氧化时溶液中反应的离子方程式为________________________ ,若流程中取消“加入MnO2”,对上述流程的影响是________________________________________。
(3)试剂X________(填“能”或“不能”)选用氢氧化锰,试说明理由:____________
______________________________________________________________________________。
(4)滤渣的主要成分是________,利用滤渣能提取铁红,其原理是______________________
______________________________________________________________________________。
(5)从滤液中提取MnSO4.H2O晶体的操作是____________________________________。
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
(15分)为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②C和CO的燃烧热(△H)分别为-393.5kJ·mol-1和-283kJ·mol-1
则2NO(g+2CO(g)=N2(g)+2CO2(g)) △H= kJ·mol-1
(2)将0.20 mol NO和0.10 mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。

①CO在0-9min内的平均反应速率v(CO)=________mol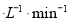 (保留两位有效数字);第12 min时改变的反应条件可能为________。
(保留两位有效数字);第12 min时改变的反应条件可能为________。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第24 min时达到平衡状态,CO2的体积分数为________(保留三位有效数字),化学平衡常数K=________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=________(用含硫微粒浓度的代数式表示)。
(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2。已知常温下0.1 mol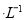 的HCOONa溶液pH =10,则HCOOH的电离常数
的HCOONa溶液pH =10,则HCOOH的电离常数 =_________。
=_________。
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
【化学——选修2:化学与技术】(15分)
通过海水能获得淡水、食盐、镁等,食盐可进一步用于氯碱工业。请回答下列问题。
(1)列举两种海水淡化的方法:_________、_________。
(2)氯碱工业通过电解饱和食盐水能获得烧碱和氯气等物质,该反应的化学方程式为_____________,如图是用离子交换膜法电解饱和食盐水的原理示意图。其中石墨接电源_________极,电解时铁电极的电极反应式为_________。电解过程中通过离子交换膜的主要离子是__________。

(3)侯氏制碱法中,首先向饱和食盐水中通入CO2和NH3制备NaHCO3,其化学方程式为____________;先通入的是__________(填化学式),其理由是__________________ ;再利用NaHCO3受热分解可制备纯碱。
(4)目前世界上60%以上的镁都是从海水中提取的,已知:MgO和MgCl2的熔点分别为2852℃和714℃。分析说明工业上采用电解熔融MgCl2而不是电解熔融MgO的理由__________ ______________________________________________________________________ 。
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
(15分)
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素。M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子。请回答下列问题:
(1)元素Q的名称为__________,P的基态原子价层电子排布式为__________ 。
(2)O的氢化物的沸点比其上一周期同族元素的氢化物低,是因为__________________________.
(3)M、O电负性大小顺序是__________(用元素符号表示),O的最高价含氧酸根的空间构型为__________,其中心原子的杂化类型为___________。
(4)M、N形成的化合物的晶胞如图所示,该晶胞的化学式为__________ ,其中M离子的配位数为__________,该晶体类型为___________。
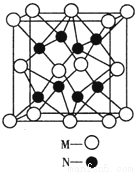
(5)该晶胞的边长为a×10 cm,则距离最近的M、N离子间的距离为
cm,则距离最近的M、N离子间的距离为
__________cm。
查看答案和解析>>
科目: 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
【化学——选修5:有机化学基础】(15分)
有机化合物A的分子式为C4H9Br,A分子的核磁共振氢谱有3个吸收峰,其面积之比为2:1:6,利用A按照下列合成路线可以合成调味剂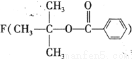 ,注:部分物质省略。
,注:部分物质省略。

已知:①B在一定条件下可以合成一种高分子化合物,C和D互为同分异构体;
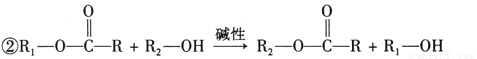
试回答下列问题:
(1)化合物B的系统命名是__________,B生成高分子化合物的化学方程式为__________
____________________________________________________________.
(2)D的结构简式为________________________。
(3)由B经两步反应转化为C经历的反应类型为__________ 和___________。
(4)E转化为F的化学方程式为_________。
(5)F的同分异构体需符合下列条件:①分子中含有苯环,苯环上共有2个取代基,且处于对位;②能与溶液反应生成CO2。符合条件的同分异构体共有_________种,其中一种异构体的核磁共振氢谱只有5个吸收峰,且吸收峰面积之比为3:2: 2:1:6,则该异构体的结构简式为 __________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com