
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
已知:t ℃时,2H(g)+Y(g)  2I(g) ΔH=-196.6 kJ·mol-1,t ℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,Y剩余0.2 mol。若在上面的平衡体系中,再加入1 mol气态的I物质,t ℃时达到新的平衡,此时H物质的物质的量n(H)为
2I(g) ΔH=-196.6 kJ·mol-1,t ℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,Y剩余0.2 mol。若在上面的平衡体系中,再加入1 mol气态的I物质,t ℃时达到新的平衡,此时H物质的物质的量n(H)为
A.0.2mol B.0.5 mol C.0.6 mol D.0.8 mol
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
2N2O5(g)  4NO2(g)+O2(g) ΔH>0 ;T1温度下的部分实验数据为:
4NO2(g)+O2(g) ΔH>0 ;T1温度下的部分实验数据为:
t/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)/mol/ L | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500 s内N2O5分解速率为2.96×10-3 mol/(L·s)
B.T1温度下的平衡常数为K1=125,1 000 s时N2O5转化率为50%
C.其他条件不变时,T2温度下反应到1 000 s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
常温下,99mL0.1mol/L的盐酸和101mL0.05mol/L氢氧化钡溶液混合后,溶液的c(H+)为(不考虑混合时的体积变化)
A.0.5×(10-8+10-10)mol/L B.(10-8+10-10)mol/L
C.(1×10-14-5×10-5)mol/L D.1×10-11 mol/L
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示。

据图判断正确的是
A.Ⅱ为盐酸稀释时的pH值变化曲线
B.b点酸的总浓度大于a点酸的总浓度
C.a点Kw的数值比c点Kw的数值大
D.b点溶液的导电性比c点溶液的导电性强
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
常温下,将0.02 mol·L-1的Ba(OH)2溶液100 mL和0.02 mol·L-1的NaHSO4溶液100 mL混合,若忽略溶液体积变化,则混合后的溶液
A.由水电离产生的c(H+)=1.0×10-2 mol·L-1
B.pH=12
C.pH=2
D.混合后的溶液溶质的物质的量浓度为0.02 mol·L-1
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
将2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:
2A(g)+3B(g)  2C(g)+zD(g),若2分钟后达到平衡,A的转化率为50%,测得:v(D)=0.25 mol/(L·min),则下列推断正确的是
2C(g)+zD(g),若2分钟后达到平衡,A的转化率为50%,测得:v(D)=0.25 mol/(L·min),则下列推断正确的是
A.v(C)=0.2 mol/(L·min)
B.z=3
C.B的转化率为25%
D.C的体积分数约为28.6%
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
如图所示,向A中充入1 mol X和1 mol Y,向B中充入2 mol X和2 mol Y,起始VA=VB=a L,在相同温度和有催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g) 2N(g)+W(g) ΔH>0,达到平衡时,v(A)=1.2aL,则下列说法错误的是
2N(g)+W(g) ΔH>0,达到平衡时,v(A)=1.2aL,则下列说法错误的是

A.反应开始时,B容器中化学反应速率快
B.A容器中X的转化率为40%,且比B中X的转化率小
C.打开K达新平衡后,升高B容器温度,A容器体积会增大
D.打开K一段时间,达到新平衡时,A的体积为2.6aL(两边通管中气体体积不计)
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g)  CH3OH(g) ΔH < 0。按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
CH3OH(g) ΔH < 0。按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
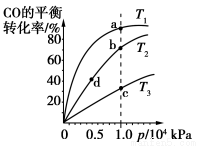
A.正反应速率:v(a)>v(c) v(b)>v(d)
B.平衡时a点一定有n(CO):n(H2)=1:2
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量: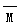 (a)<
(a)< 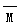 (c)
(c) 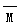 (b)>
(b)> 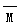 (d)
(d)
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:填空题
(8分)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:(按照要求用 a、 b 、c表示)
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________________。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是______________。
(3)当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是________________。
(4)若三者c(H+)相同时,物质的量浓度由大到小的顺序是________________。
(5)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是____________。
(6)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为________,反应所需时间的长短关系是_________
(7)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是_________________。
查看答案和解析>>
科目: 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:实验题
(10分)某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视________,直到因加入一滴盐酸后,溶液由黄色变为橙色,并____________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是________(填字母序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为________mL。

(4)某学生根据3次实验分别记录有关数据如下表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度。(保留4位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com