
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:选择题
下列实验操作正确且能达到预期目的的是
| 实验目的 | 操作 |
A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入酸性KMnO4溶液,看紫红色是否褪去 |
C | 确定碳、氯两元素非金属性的强弱 | 测定同温同浓度的Na2CO3和NaClO水溶液的pH |
D | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
查看答案和解析>>
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:选择题
已知:25 ℃时,CaCO3的Ksp=2.8×10-9,CaCO3在水中的溶解平衡曲线如图所示。下列说法正确的是

A.x数值为1.4×10-5
B.b点与d点对应的溶度积相等
C.加入蒸馏水可使溶液由d点变到a点
D.c点将有沉淀生成,平衡后溶液中c(Ca2+)、c(CO32-)一定相等
查看答案和解析>>
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:选择题
已知X、Y、Z、W是原子序数依次增大的短周期元素,这些元素的其他信息如下表。下列说法正确的是
元素 | 信息 |
X | K层电子数是L层电子数的2倍 |
Y | 一种核素在考古时常用来鉴定一些文物的年代 |
Z | 所处的周期序数与族序数相等 |
W | 最高价氧化物对应的水化物酸性最强 |
A.W的阴离子半径大于Z的阳离子半径
B.Y的氢化物比W的氢化物稳定
C.Z的最高价氧化物对应的水化物不能够溶于Y的最高价氧化物对应的水化物
D.X在氧气中加热反应生成X2O2
查看答案和解析>>
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:选择题
常温下,pH=12的NaOH溶液和pH=2的醋酸混合后恰好完全反应(不考虑溶液体积的变化)。下列说法正确的是
A.反应后的溶液呈酸性
B.两种反应物中水电离出的c(H+)都是1×10-12 mol·L-1
C.反应后的溶液中:c(CH3COO-)+c(CH3COOH)=0.01mol·L-1
D.反应后的溶液中:c(Na+) >c(CH3COO-)>c( OH-)>c(H+)
查看答案和解析>>
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:推断题
(16分)钯/碳高效绿色催化Suzuki 交叉偶联反应是近年来有机合成的热点之一,如反应①:
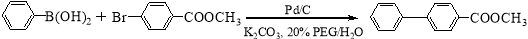
I II
化合物Ⅱ可由化合物III合成:

(1)化合物Ⅱ的分子式为 ,含有的官能团名称为 。
(2)化合物Ⅳ的结构简式为 。
(3)化合物Ⅵ与新制Cu(OH)2悬浊液反应的化学方程式为 (注明条件)。
(4)化合物Ⅴ的一种同分异构体Ⅷ遇FeCl3溶液显紫色,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为 _________ 。写出化合物Ⅷ与足量NaOH水溶液反应的化学方程式为 (注明条件)。
(5)化合物 与化合物
与化合物 在一定条件可发生类似反应①的反应,其产物的结构简式为 。
在一定条件可发生类似反应①的反应,其产物的结构简式为 。
查看答案和解析>>
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:简答题
(15分)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)= 。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
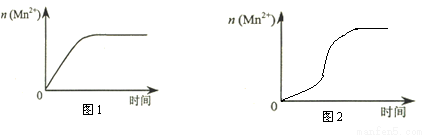
①该小组同学提出的假设是 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05 mol/L KMnO4溶液 | |||
4 | 3.0 | 2.0 | 2.0 | 3.0 |
| t |
③若该小组同学提出的假设成立,应观察到的现象是 。
(4)工业上可用电解K2MnO4浓溶液的方法制取KMnO4,则电解时,阳极发生的电极反应为 ;总方程式为 。
查看答案和解析>>
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:实验题
(16分)利用钛白工业的副产品FeSO4(含TiO2+、Al3+)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
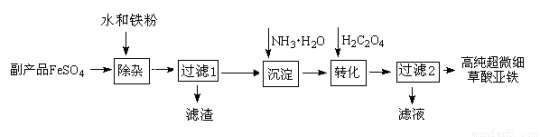
(1)检验FeSO4是否已有部分氧化的方法是 。
(2)已知过滤1得到的滤渣的主要成分是Al(OH)3、H2TiO3。请补充化学方程式:
TiOSO4 + =H2SO4 + H2TiO3↓;铁粉的作用有:①除去溶液中的Fe3+,② 。
(3)沉淀反应的离子方程式是 。
(4)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有 。FeC2O4生成后,为提高产品纯度,还需调节溶液pH=2,若pH过低,则导致FeC2O4的产率______(填“偏高”、“偏低”或“无影响”)。
(5)过滤2得到的滤液经蒸发浓缩、 、洗涤可得到副产品,该物质可用作 (写出一种用途)。
查看答案和解析>>
科目: 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:实验题
(17分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:

称取研细的黄铜矿样品1.150g,在空气存在的条件下进行煅烧。实验后取d中溶液的1/10置于锥形瓶中,用0.05mo1/L标准碘溶液进行滴定,初读数为0.10mL,终读数如右上图所示。
(1)黄铜矿煅烧的反应为8CuFeS2+21O2高温8Cu+4FeO+2Fe2O3+16SO2,该反应中被还原的元素是___(填元素符号)。
(2)标准碘溶液应盛放在(填“碱式”或“酸式”)________滴定管中;装液之前,滴定管要用标准碘溶液润洗2—3次,润洗的操作是: 。请用化学方程式表示滴定的原理: 。
(3)滴定终点的读数为 mL;通过计算可知,该黄铜矿的纯度为 。
(4)若去掉c装置,会使测定结果 (填“偏低”“偏高”或“无影响”)。
(5)假设实验操作均正确,测得黄铜矿的纯度偏低,可能的原因主要有 。
查看答案和解析>>
科目: 来源:2013-2014广东省梅州市高一下学期期中化学试卷(解析版) 题型:选择题
对发现元素周期律贡献最大的化学家是 ( )
A.牛顿 B.道尔顿 C.阿伏加德罗 D.门捷列夫
查看答案和解析>>
科目: 来源:2013-2014广东省梅州市高一下学期期中化学试卷(解析版) 题型:选择题
下列叙述中正确的是( )
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B. 除短周期外,其他周期均有18种元素
C.副族元素中没有非金属元素
D.碱金属元素是指IA族的所有元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com