
科目: 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:填空题
(12分)下图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下的气态化合物,C为常温下的液态化合物,图中有部分生成物未标出。
请填写以下空白:

(1)A的化学式为 ,B的电子式为 。
(2)写出下列反应的化学方程式:
D+G→H 。
F+J→B+C+I 。
(3)0.3 mol I与足量C反应转移电子的物质的量为 mol。
(4)容积为10 mL的试管中充满I和G的混合气体,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I与G的体积分别为 mL, mL。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:填空题
随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具体有重要意义。
(1)如图是在101 kPa,298K条件下1mol NO2和1mol CO反应生成1mol CO2和1mol NO过程中的能量变化示意图。
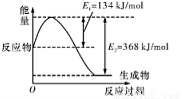
已知:
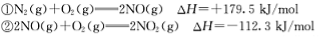
请写出NO与CO反应生成无污染气体的热化学方
程式: 。
(2)将0.20 mol N02和0.10 mol CO充入一个容积恒定为1L的密闭容器中发生反应,在不同条件下,反应过程中部分物质的浓度变化状况如图所示。
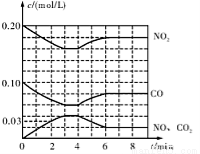
①下列说法正确的是 (填序号)。
a.容器内的压强不发生变化说明该反应达到乎衡
b.当向容器中再充人0. 20 mol NO时,平衡向正反应方向移动,K增大
c.升高温度后,K减小,N02的转化率减小
d.向该容器内充人He气,反应物的体积减小,浓度增大,所以反应速率增大
②计算产物NO在0~2 min内平均反应速率v(NO)= mol·L-1·min-1
③第4 min时改变的反应条件为 (填“升温’’、“降温’’)。
④计算反应在第6 min时的平衡常数K= 。若保持温度不变,此时再向容器中充人CO、NO各0.060 mol,平衡将 移动(填“正向”、“逆向”或“不”)。
(3)有学者想以如图所示装置用原电池原理将SO2转化为重要的化工原料。其负极反应式为 ,当有0.25 mol SO2被吸收,则通过质子(H+)交换膜的H+的物质的量为 mol。

查看答案和解析>>
科目: 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:实验题
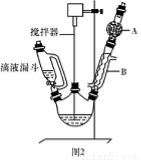
三苯甲醇(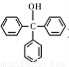 )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图所示。
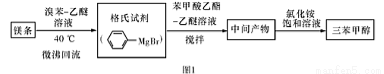
已知:(I)格氏试剂容易水【解析】
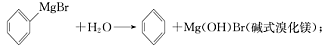
(Ⅱ)相关物质的物理性质如下:
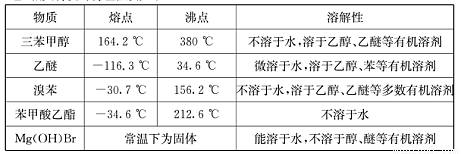
(Ⅲ)三苯甲醇的相对分子质量是260,纯净固体有机物一般都有固定熔点。
请回答以下问题:
(1)图2中玻璃仪器B的名称: ;装有无水CaCl2的仪器A的作用是 。
(2)图2中滴加液体未用普通分液漏斗而用滴液漏斗的作用是 ;制取格氏试剂时要保持微沸,可以采用 加热方式。
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写如下空白:

其中,①操作为: ;洗涤液最好选用 (从以下选项中选择);
A.水 B.乙醚 C.乙醇 D.苯
检验产品已经洗涤干净的操作为: 。
(4)纯度测定:称取2.60 g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不反应),充分反应后,测得生成的气体在标准状况下的体积为100.80mL。则产品中三苯甲醇的质量分数为 。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:填空题
海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河人海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和 池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用:
(写一点即可)。
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:

①海水不能直接通人到阴极室中,理由是 。
②A口排出的是 (填“淡水”或“浓水”)。
(3)用苦卤(含Na+、K+、Mg2+、Cl-、Br-等离子)可提取溴,其生产流程如下:

①若吸收塔中的溶液含Br03-,则吸收塔中反应的离子方程式为: 。
②通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液?
③向蒸馏塔中通入水蒸气加热,控制温度在90℃左右进行蒸馏的原因是
查看答案和解析>>
科目: 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:填空题
(1)主族元素A的简单阳离子不与任何原子具有相同的核外电子排布。元素B与氮元素同周期,B的原子序数大于氮,而第一电离能比氮的小。A与B能形成两种化合物A2B2和A2B,其中B的杂化方式分别为 、 。A2B、NH3、SiH4的键角由大到小依次为 (填化学式)。A2B由液态形成晶体时密度减小,主要原因是 。
(2)新型无机材料在许多领域被广泛应用。陶瓷发动机的材料选用氮化硅,它硬度大、化学稳定性强,是很好的高温陶瓷材料。除氢氟酸外,氮化硅不与其他无机酸反应,抗腐蚀能力强。氮化硅的晶体类型是 ,氮化硅与氢氟酸反应的化学方程式为 。
(3)MgC03和CaC03都为离子晶体,热分解的温度分别为402℃和900℃,请根据结构与性质的关系说明它们热分解温度不同的原因: 。
(4)砷化镓广泛用于雷达、电子计算机、人造卫星、宇宙飞船等尖端技术中。镓的基态原子价电子排布式为 ,砷化镓的晶胞结构与金刚石相似,其晶胞边长为a pm,则每立方厘米该晶体中所含砷元素的质量为 g(用NA表示阿伏加德罗常数)。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:填空题
肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体。
(1)肉桂酸甲酯由C、H、O三种元素组成,质谱分析其分子的相对分子质量为162,核磁共振氢谱谱图显示有6个峰,其面积之比为1:2:2:1:1:3,利用红外光谱仪检测其中的某些基团,测得红外光谱如下图:

则肉桂酸甲酯的结构简式是 (不考虑立体异构)
(2)已知:
I.醛与醛能发生反应,原理如下:

Ⅱ.已知烃A在标准状况下的密度为1.25g.L-1。合成肉桂酸甲酯的工业流程如下图所示:

请回答:
①化合物J的结构简式为 ;
②化合物G中的官能团有 ;
③G→H为 反应(填反应类型);
④写出反应D→E的化学方程式 ;
H→I的反应 (填“能”或“不能”)改用酸性高锰酸钾溶液,简述理由: 。
⑤符合下列条件的I的同分异构体共有5种。写出另两种同分异构体的结构简式:
A.能发生水解反应
B.与银氨溶液作用出现光亮的银镜
C.能与溴发生加成

查看答案和解析>>
科目: 来源:2013-2014学年湖南省益阳市高三下学期模拟考试理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列叙述中不正确的是
A.户外钢架桥生锈主要是电化学腐蚀所致
B.导电塑料是应用于电子工业的一种新型有机高分子材料
C.CO2、NO2或SO2都会导致酸雨的形成
D.葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒
查看答案和解析>>
科目: 来源:2013-2014学年湖南省益阳市高三下学期模拟考试理综化学试卷(解析版) 题型:选择题
莽草酸的结构简式如下图所示,可用来合成药物达菲,下列关于莽草酸的说法错误的是

A.分子式为C7H10O5
B.分子中含有两种官能团
C.既可发生加成又可发生取代反应
D.能够使酸性高锰酸钾溶液和溴水褪色
查看答案和解析>>
科目: 来源:2013-2014学年湖南省益阳市高三下学期模拟考试理综化学试卷(解析版) 题型:选择题
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,下列结论正确的是
W | X |
|
| Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Z
B.Z元素氧化物对应水化物的酸性一定强于Y
C.Z元素单质在化学反应中只表现氧化性
D.X、Y、Z元素形成的单核阴离子还原性最强的是Y
查看答案和解析>>
科目: 来源:2013-2014学年湖南省益阳市高三下学期模拟考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
①常温常压下,18g14CH4所含中子数目为8 NA
②1L0.1mol·L-1的氨水中有NA个NH4+
③1mol Na2O2中含有NA个阴离子
④1L1mol·L-1NaClO 溶液中含有ClO-的数目为NA
⑤78g 苯含有C=C双键的数目为3NA
⑥0.1molN2和0.3molH2在某密闭容器中充分反应,转移电子的数目为0.6NA
⑦60gSiO2晶体中含有硅氧键的数目为4NA
A.①③⑦ B.②③⑥ C.②④⑥ D.①④⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com