
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.常温常压下,1.7gH2O2中含有的电子数为0.9NA
B.1 mol.L-1CuCl2溶液含有2NA个Cl-
C.1 mol Na 与足量 O2反应,生成Na2O和Na2O2的混合物,钠失去2NA个电子
D.标准状况下,2.24L戊烷所含分子数为0.1NA
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
在水溶液中能大量共存的一组是( )
A.Ba2+、Na+、SO32-、Cl? B.MnO4? 、SO42? 、K+ 、H+
C.Al3+ 、Mg2+、NO3? 、HCO3? D.Fe3+、Na+、SCN? 、Cl?
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.碳酸氢钠溶液可用于区分乙酸、乙醇和苯
B.糖类、油脂、蛋白质都是高分子化合物,都可以在一定条件下发生水解反应
C.用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
短周期元素X、Y、W、Q在元素周期表中的相对位置如图所示.常温下,Al能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液.下列说法正确的是( )

A.Y的最高化合价为+6
B.离子半径:W>Q>Y>X
C.氢化物的沸点:Y>Q
D.最高价氧化物的水化物的酸性:W>Q
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH—2e—→X+2H+.下列说法中正确的是( )
A.电池内部H+由正极向负极移动
B.另一极的电极反应式为:O2+4e—+2H2O=4OH—
C.乙醇在正极发生反应,电子经过外电路流向负极
D.电池总反应为:2CH3CH2OH + O2→2CH3CHO + 2H2O
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
下列有关物质的性质与其应用不相对应的是( )
A.Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品
B.NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂
C.NH3能与Cl2生成NH4Cl,可用浓氨水检验输送氯气的管道是否有泄漏
D.K2FeO4能与水作用生成Fe(OH) 3胶体和O2,可用于自来水的净化和杀菌消毒
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
25℃时,下列说法正确的是( )
A.氨水与氯化铵的pH=7的混合溶液中:c(Cl—)>c(NH4+)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3—) >c(H2CO3)>c(CO32?)
C.pH=12的NaOH溶液与等体积pH=2的醋酸溶液混合后所得溶液显酸性
D.将0.1 mol/L的氨水溶液加水稀释10倍,溶液中离子浓度都减少
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(如图)就能实现相应实验目的是( )
选项 | A | B | C | D |
实验目的 | 从碘水中提取碘 | 用10mol?L-1盐酸配制100mL 0.1mol?L-1盐酸 | 用NaCl溶液制备氯化钠晶体 | 除去C2H4中少量SO2 |
实验仪器或装置 | 烧杯、分液漏斗 | 100mL容量瓶、量筒、玻璃棒、烧杯 |
|
|
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:推断题
化合物Ⅳ为一种重要化工中间体,其合成方法如下:

(1)化合物Ⅱ的分子式为_______________;反应②的反应类型为________________。
化合物IV中含有的官能团是 。(写名称)
(2)化合物I在NaOH醇溶液中加热反应,生成两种有机化合物(互为同分异构体),请写出任意一种有机化合物的结构简式:______________
(3)1mol化合物III与足量NaOH反应消耗NaOH的物质的量为 mol。
(4)化合物IV在浓硫酸催化下反应生成六元环状酯类化合物,写出该反应的化学方程式 ________________。
(5)根据题给化合物转化关系及相关条件,请你推出 (2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物VI和VII,结构简式分别是为 、 ,它们物质的量之比是 。
(2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物VI和VII,结构简式分别是为 、 ,它们物质的量之比是 。
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:填空题
对大气污染物SO2、NOx进行研究具有重要环保意义。请回答下列问题:
(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。
已知:① H2(g)+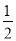 O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1
②C(s)+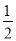 O2(g)=CO(g) △H=-110.5kJ·mol-1
O2(g)=CO(g) △H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式: 。
(2)已知汽车汽缸中生成NO的反应为:N2(g)+O2(g) 2NO(g) △H
2NO(g) △H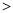 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
①在1300oC 时,该反应的平衡常数表达式K= 。5s内该反应的平均速率ν(N2) = (保留2位有效数字);
②汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
(3)汽车尾气中NO和CO的转化。当催化剂质量一定时,增大催化剂固体的表面积可提高化学反应速率。下图表示在其他条件不变时,反应2NO(g)+2CO(g)  2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
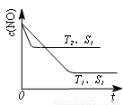
①该反应的△H 0 (填“>”或“<”)。
②若催化剂的表面积S1>S2,在右图中画出c(NO) 在T1、S2条件下达到平衡过程中的变化曲线(并作相应标注)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com