
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:选择题
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH值:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
下列说法或表达中,正确的是
A.少量二氧化碳通入NaClO溶液中:2NaClO + CO2 + H2O Na2CO3 + 2HClO
Na2CO3 + 2HClO
B.过量的 HCN滴入碳酸钠溶液中 HCN + Na2CO3 NaCN+ NaHCO3
NaCN+ NaHCO3
C.结合质子能力由强到弱的顺序为:CO32—>CN—>HCO3—>CH3COO—
D.常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN)
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:选择题
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,如附图所示流程处理,下列说法中,正确的是
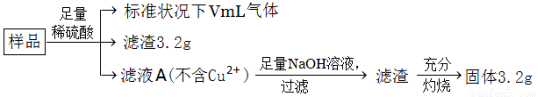
A.滤液A中阳离子为Fe2+、H+
B.样品中金属Fe的质量为2.14g
C.样品中CuO的质量为4.0g
D.V=448
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:填空题
氮元素广泛存在于自然界中,对人类生命和生活具有重要意义。含氮元素的化合物在工业生产和国防建设中都有广泛的应用。
(1)氮元素原子核外有 个未成对电子,最外层有 种能量不同的电子。PH3分子的空间构型为 ,是 分子。(填极性或非极性)
(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是 (填编号)
a.NH3比PH3稳定性强
b.硝酸显强氧化性,磷酸不显强氧化性
c.氮气与氢气能直接化合,磷与氢气很难直接化合
d.氮气常温是气体,磷单质是固体
亚硝酸盐是食品添加剂中急性毒性较强的物质之一,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。
(3)亚硝酸钠溶液滴加到K2Cr2O7酸性溶液中,溶液由橙色变为绿色,反应如下,补上缺项物质并配平:
Cr2O72- + NO2- + → Cr3+ + NO3-+
(4)上题反应中每消耗0.6mol NO2-,转移电子数为 。
(5)氮氧化物(NO和NO2)污染环境。若用Na2CO3溶液吸收NO2可生成CO2,9.2gNO2和Na2CO3溶液完全反应时转移电子0.1 mol,则反应的离子方程式为 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:填空题
工业制硫酸的过程中利用反应2SO2(g)+O2(g) 2SO3(g)+Q (Q>0),将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
2SO3(g)+Q (Q>0),将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
(1)写出该可逆反应的化学平衡常数表达式 ;
(2)一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2发生反应,下列说法中,正确的是 (填编号)。
a.若反应速率υ正(O2)=2υ逆(SO3),则可以说明该可逆反应已达到平衡状态
b.保持温度和容器体积不变,充入2 mol N2,化学反应速率加快
c.平衡后移动活塞压缩气体,平衡时SO2、O2的百分含量减小,SO3的百分含量增大
d.平衡后升高温度,平衡常数K增大
将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | |||
1 | T1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | 4 | 2 | 0.4 | y | t |
(3)实验1从开始到反应达到化学平衡时,υ(SO2)表示的反应速率为 ;
T1 T2 (选填“>”、“<”或“=”),理由是 。尾气SO2用NaOH溶液吸收后会生成Na2SO3。现有常温下0.1mol/LNa2SO3溶液,实验测定其pH约为8,完成下列问题:
(4)该溶液中c(Na+)与 c(OH-) 之比为 。
该溶液中c(OH—) = c(H+)+ + (用溶液中所含微粒的浓度表示)。
(5)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是 (用编号排序)
A.Na2SO3 B.Ba(NO3)2 C.Na2S D.酸性KMnO4
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:实验题
我国化工专家侯德榜,勇于创新,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。请完成下列问题:
(1)“联合制碱法”制得的“碱”是 (填化学式)。
(2)氨碱法和联合制碱法是两大重要的工业制碱法,下列表达中,不正确的是 。
|
| 氨碱法 | 联合制碱法 |
A | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
B | 可能的副产物 | 氯化钙 | 氯化铵 |
C | 循环物质 | 氨气、二氧化碳 | 氯化钠 |
D | 评价 | 原料易得;设备复杂;能耗高 | 原料利用率高;废弃物少 |
某实验小组,利用下列装置模拟“联合制碱法”。
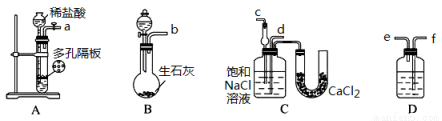
(3)取上述仪器连接装置,顺序为:(a)接( )、( )接( );(b)接( );
检验气密性后装入药品,应该先让 装置(填上述字母)先发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体。
(4)C中用球形干燥管而不用直导管,其作用是 ,D中应选用的液体为 ;
(5)C中广口瓶内产生固体的总化学方程式为 。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为: (注明你的表达式中所用的有关符号的含义)。
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:填空题
辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
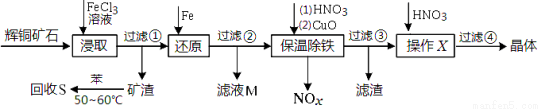
(1)写出步骤“还原”中可能发生反应的离子方程式 、 。
(2)回收S过程中温度控制50℃~60℃之间,不宜过高或过低的原因是 、 。
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该物质的化学式为 ;向滤液M中加入(或通入)下列 (填字母)物质,得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾 d.盐酸
(4)保温除铁过程中加入CuO的目的是 、 ;
(5)过滤③所得到的滤液,加入硝酸后,经操作X、过滤④得到硝酸铜晶体。
硝酸的作用是 ;
操作X是 、 (填操作名称) 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:填空题
有机物A ( 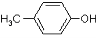 )是有机工业的重要原料,可用于合成多种有机物。
)是有机工业的重要原料,可用于合成多种有机物。
I.由A为原料,可以合成有机物D。根据如下流程回答:
已知:R-CN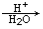 R-COOH。
R-COOH。
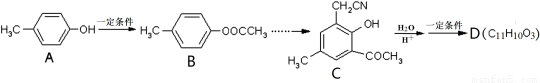
(1)A的名称为 ;
(2)D的结构简式为 。
II.以A为主要原料合成有机物G: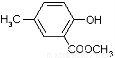 ,合成路线流程图为:
,合成路线流程图为:
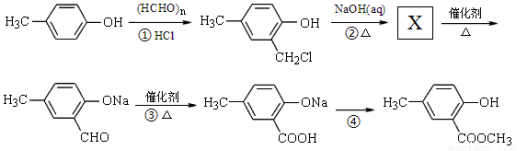
(3)反应②的化学方程式 ;
(4)写出检验反应③的产物中残留有机反应物的试剂 ;
(5)写出符合下列条件的G的同分异构体的其中一种结构简式:①分子中含有苯环,且苯环上一氯代物只有一种;②能发生水解反应;③遇FeCl3溶液显紫色。 。
(6)根据已有知识并结合相关信息,写出以A的最简单同系物为原料制备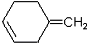 的合成路线流程图表示(有机物用结构简式,注明反应试剂和条件)
的合成路线流程图表示(有机物用结构简式,注明反应试剂和条件)
(合成路线常用的表示方式为:A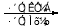 B……
B……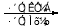 目标产物)
目标产物)
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:填空题
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化为烃B、烃C。以C为原料可以合成聚对羟基苯甲酸 (G)。已知:
①A是一种有机酸,分子式为C9H10O3。
②B的相对分子质量为104,分子中含苯环且能使溴的四氯化碳溶液褪色。
③C的相对分子质量为78,且分子中只有一种氢原子。
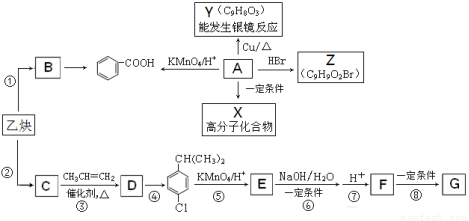
(1)写出乙炔分子的电子式 , F中的含氧官能团名称 ;
(2)上述①至⑧的反应中,属于加成反应的有 ,第④步反应所需的试剂和条件是 ;
(3)写出A的结构简式 ;
(4)下列有关的描述中,正确的是 ;
a. 1molB最多能与4molH2加成
b. B通过氧化反应可使溴水和酸性KMnO4溶液褪色
c. B、C、D是同系物
d. A→X的反应属于缩聚反应
(5)写出F→G反应的化学方程式 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三二模化学试卷(解析版) 题型:填空题
氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和Cu。
(1)现有8.4克氧化铜被氢气完全还原后,得到红色固体6.96克,其中含单质铜与氧化亚铜的物质的量之比是 ;
(2)若将6.96克上述混合物与足量的浓硝酸充分反应:
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体20.328g。经分析,原溶液中的Cu2+有20%残留在母液中,所得晶体的化学式为 。
(3)Cu、Cu2O和CuO组成的混合物,加入100mL 0.6mol/L HNO3溶液恰好使混合物完全溶解,同时收集到224mL NO气体(标准状况)。如原混合物中Cu的物质的量为X,求其中Cu2O、CuO的物质的量及X的取值范围(写出解题过程)。
查看答案和解析>>
科目: 来源:2013-2014学年北京市丰台区高三下学期统一练习(一)化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是
A.食盐可作调味剂 B.CO2属于大气污染物
C.柠檬很酸,属于酸性食物 D.用聚氯乙烯塑料袋包装食品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com