
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:选择题
在0.1 mol/L的NaHSO3溶液中有如下关系:c(Na+)>c(HSO3-) >c(SO32-) >c(H2SO3),向NaHSO3溶液中慢慢地加入少量的NaOH溶液,发生的主要反应的离子方程式为
A.SO32-+H2O HSO3-十OH— B.HSO3-十H2O
HSO3-十OH— B.HSO3-十H2O H2SO3十OH-
H2SO3十OH-
C.HSO3-十OH— SO32—十H2O D.H2SO3+OH-
SO32—十H2O D.H2SO3+OH- HSO3-十H2O
HSO3-十H2O
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:选择题
在含有n mol FeI2的溶液中通入Cl2,有x mol Cl2发生反应。下列说法正确的是
A.当x ≤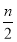 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl-
时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl-
B.当x ≥ n时,反应的离子方程式为:2Fe2++ 2I-+ 2Cl2 → 2Fe3++ I2+ 4Cl-
C.当Fe2+和I-同时被氧化时,x与n的关系为x>n
D.当x=n时,反应后氧化产物的物质的量为n mol
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:选择题
将气体A2和B2以等物质的量充入密闭容器,一定条件下发生反应生成C气体。平衡时测得c(A2)= 0.58 mol/L,c(B2)=0.16 mol/L,c(C)=0.84 mol/L,则C的分子式为
A.AB B.AB2 C.A2B D.A2B3
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:填空题
液化石油气中常存在少量有毒气体羰基硫(COS),必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。
(1)写出羰基硫的电子式 ,羰基硫分子属于 (选填“极性”、“非极性”)分子。
(2)下列能说明碳与硫两元素非金属性相对强弱的是 。
a.相同条件下水溶液的pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
(3)羰基硫在水存在时会缓慢水解生成H2S,对钢铁设备产生电化学腐蚀。写出正极的电极反应式 ,负极的反应产物为 (填化学式)。
为除去羰基硫,工业上常采用催化加氢转化法,把羰基硫转化为H2S再除去:COS + H2  CO + H2S
CO + H2S
(4)已知升高温度,会降低羰基硫的转化率。则升高温度,平衡常数K ,反应速率 (均选填“增大”、“减小”、“不变”)。
(5)若反应在恒容绝热密闭容器中进行,能说明该反应已达到平衡状态的是 。
a.容器内气体密度保持不变 b.容器内温度保持不变
c.c(H2)=c(H2S) d.υ(H2)正=υ(H2S)正
(6)已知该反应的平衡常数很大,说明 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:填空题
铁及其化合物在生产、生活中存在广泛用途,完成下列填空。
(1)如图所示为铁元素在周期表中的信息,方格中“55.85”的意义为: 。铁原子核外有 种运动状态不同的电子。

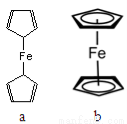
(2)二茂铁[Fe(C5H5)2]是一种有机金属化合物,熔点172℃,沸点249℃,易升华,难溶于水易溶于有机溶剂。二茂铁属于 晶体;测定表明二茂铁中所有氢原子的化学环境都相同,则二茂铁的结构应为图中的 (选填“a”或“b”)。
(3)绿矾(FeSO4·7H2O)可用于治疗缺铁性贫血,其水溶液露置于空气中会变质,
写出发生变质反应的离子方程式 。
(4)无水FeCl3是水处理剂,遇潮湿空气即产生白雾,易吸收空气中的水分成为结晶氯化铁(FeCl3·6H2O)。制备无水FeCl3的试剂是 。
(5)高铁酸盐也是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:
2FeSO4 + 6Na2O2 → 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,若生成2mol Na2FeO4,则反应中电子转移的物质的量为 mol。
(6)高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含 Mn2+ 1mg的水体样本,需要1.2 mg/L高铁酸钾 L。
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:实验题
某研究性学习小组通过下列实验探究SO2能否与BaCl2溶液反应生成BaSO3沉淀,并制备硫酸铜晶体。完成下列填空。甲同学用装置I进行实验,加热反应物至沸腾,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸。
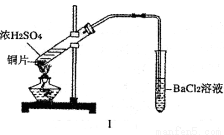
(1)白色沉淀是 。
(2)甲同学就白色沉淀的生成原因提出了两种假设,这两种假设可能是:
① ②
乙同学设计了改进装置Ⅱ进行实验,检验甲同学提出的假设(夹持装置和A中加热装置已略,气密性已检验)。
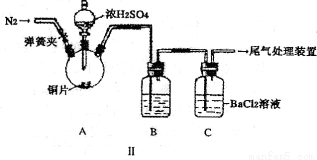
①打开弹簧夹,通入N2一段时间后关闭弹簧夹;
②滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成。
(3)操作①的目的是 ,集气瓶B中的试剂是 。
(4)该实验能否检验甲同学上述两种假设中的任意一种 ,理由是 。
丙同学向反应后的蓝色溶液中加入足量的CuO,过滤后将滤液制成硫酸铜晶体(CuSO4·xH2O),采用加热法测定该晶体中结晶水x的值,实验数据记录如下:
坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | |
第一次称量 | 第二次称量 | ||
11.710g | 22.700g | 18.621g | a |
(5)若无需再进行第三次称量,则a的数值范围应为 。
(6)若加热后坩埚与固体总质量为18.620g,计算x 的实测值 (保留二位小数),相对误差 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:填空题
为了回收利用钢铁生产过程中产生的SO2,工业上采用软锰矿(主要成分MnO2)脱硫同时制取硫酸锰技术,其流程示意图如下:
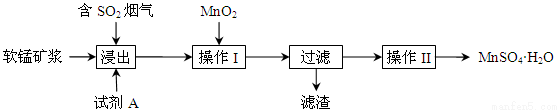
已知:浸出液的pH接近4,其中的金属离子主要是Mn2+,还含有少量的Fe2+。完成下列填空。
(1)写出浸出过程中主要反应的化学方程式: 。
(2)浸出过程的副反应之一是部分SO2被氧化为硫酸,致使浸出液的pH下降,这将 (“有利”、“不利”)于软锰矿浆继续吸收SO2。欲消除生成的硫酸,试剂A最好是 。
a.MnCO3 b.MnO2 c.CaO d.CaCO3
(3)操作I的目的是除去浸出液中的Fe2+,MnO2在氧化Fe2+的同时还 ,使Fe3+沉淀。检验过滤后溶液中是否含有Fe3+的操作是 。
(4)已知大于27℃时,MnSO4·H2O溶解度随温度上升而明显下降,则操作II的过程为: 、 、洗涤、干燥。工业上为了充分利用锰元素,在流程中 可循环使用。
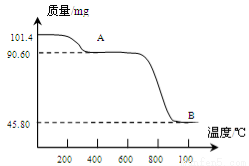
(5)通过煅烧MnSO4·H2O 可制得生产软磁铁氧体材料的MnxO4,如图是煅烧MnSO4·H2O时温度与剩余固体质量变化曲线。该曲线中A段所表示物质的化学式为 ;MnxO4中x= 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:填空题
碳酸二甲酯(DMC)是一种低毒性的绿色化学品,可用于代替高毒性的光气(COCl2)作羰基化试剂。DMC的合成路线如下图。完成下列填空。
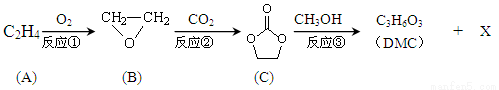
已知:RCOOR’ + R’’ OH → RCOOR’’ + R’OH
(1)写出反应类型:反应① 反应③
(2)石油工业上获得C2H4的操作名称为 。
(3)写出结构简式:DMC ; X
(4)已知物质Y与DMC互为同分异构体,Y的水溶液呈酸性,在一定条件下2 molY能生成1mol分子中含六元环结构的有机物,则Y的结构简式为:
(5)DMC与双酚( 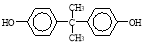 )在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式: 。
)在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式: 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:填空题
苯巴比妥是安眠药的成分,化学式为C12H12N2O3,分子结构中有两个六元环:下图是以A为原料合成苯巴比妥的流程示意图。完成下列填空。
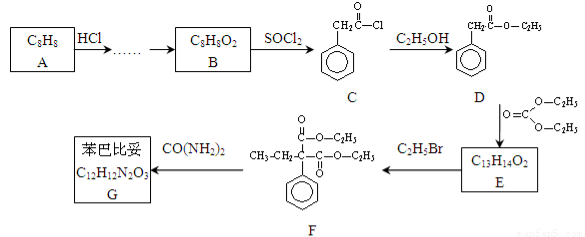
已知:①有机物D、E中亚甲基(—CH2—)的氢原子受羰基影响活性较高,容易发生如下反应:
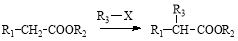
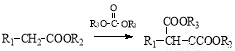
②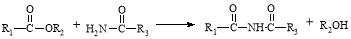
(1)芳香烃A与HCl反应后,制取B还需进行反应的类型依次为 。
(2)一种酯与B互为同分异构体,且苯环上只有一个取代基,该酯同分异构体有 种,写出其中一种结构系统命名 。
(3)写出D 转化为E的化学方程式:
(4)苯巴比妥G的结构简式:
(5)E与CO(NH2)2在一定条件下合成的高分子结构简式:
(6)已知: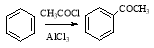 ,请设计合理方案以B的同系物
,请设计合理方案以B的同系物 为原料合成
为原料合成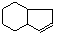 (用合成路线流程图表示为:A
(用合成路线流程图表示为:A B……
B…… 目标产物)。
目标产物)。
查看答案和解析>>
科目: 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:填空题
将CO2通入NaOH溶液中,所得产物随通入的CO2的物质的量的不同而不同。完成下列填空。
(1)250 mL 1 mol/L的NaOH溶液,最多可吸收CO2 L(标准状况下)。
(2)向250 mL 2 mol/L的NaOH溶液中通入一定量CO2,溶液增重4.4 g,将所得溶液蒸干,计算所得固体中各成分的物质的量。
向未知浓度、体积为V L的 NaOH溶液中缓缓通入一定体积(标准状况下)的CO2,充分反应后,在减压低温的条件下蒸发溶液,得到白色固体。
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1 g 白色沉淀。
①根据以上数据,用代数式表示CO2的体积V(CO2)= 。
②根据以上数据,推理计算出NaOH溶液的浓度范围。
(4)写出确定NaOH浓度的实验步骤,并用代数式表示NaOH溶液的浓度。(设计实验方案时,只能用题中提供的CO2和NaOH溶液,不得使用其它化学试剂。)
实验步骤: 。c(NaOH)= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com