
科目: 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:填空题
按要求回答下列问题:
(1) 用电子式表示H2O的形成过程________________________。
(2) 用电子式表示MgCl2的形成过程________________________。
查看答案和解析>>
科目: 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:填空题
按要求回答下列问题:
(1)硫酸铜水溶液中含有的水合铜离子化学式为________。向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液,生成深蓝色的配合离子化学式为________ ,再向反应后的溶液中加入乙醇,析出的深蓝色晶体的化学式为________ 。
(2)试比较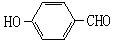 和
和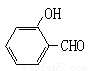 的沸点高低并说明理由_________。
的沸点高低并说明理由_________。
查看答案和解析>>
科目: 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:填空题
按要求回答下列问题:
(1)有下列六种物质:①碳60(C60)晶体②硼晶体③Na2O晶体④ CaF2晶体⑤P4O10晶体⑥碳化硅晶体。其中属于离子晶体的是 ,属于分子晶体的是 ,属于原子晶体的是____。
(2)有下列分子:HCN、P4、SO3、PCl3、BF3,其中属于非极性分子的是 。
(3)有下列离子:SO32-、SO42-、CO32-,其中VSEPR模型为正四面体形的是 ,中心原子的杂化轨道类型属于sp2杂化的是 。
(4)CaO晶胞如右图所示,CaO晶体中Ca2+的配位数为______;与每一个钙离子距离最近并且距离相等的钙离子有____个 ;CaO晶体和NaCl晶体的晶格能分别为:CaO:3 401 kJ/mol、NaCl:786 kJ/mol。导致两者晶格能差异的主要原因_______________。
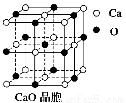
查看答案和解析>>
科目: 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:填空题
A、B、C、D、E、R六种元素位于周期表的前四周期,其原子序数依次增大。已知A原子核外有三个未成对电子;B的最外层电子数是内层电子数的3倍;化合物C2E的晶体为离子晶体;D单质的熔点在同周期单质中最高;E原子核外的M层中只有两对成对电子;R原子核外最外层电子数与C相同,其余各层均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D四种原子的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)C的氯化物的熔点比D的氯化物的熔点高,理由是 。
(3)基态R+离子的核外电子排布式是 。
(4)Q分子是A2B的等电子体,Q的结构式为 。
(5)图一是R单质的晶胞结构,配位数为 ;图二是B、R两元素组成的一种化合物的晶胞,其化学式为 。
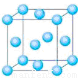
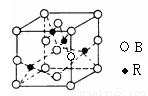
图一 图二
查看答案和解析>>
科目: 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:实验题
某校化学小组为探究铁与浓硫酸反应是否生成SO2,设计了以下装置进行实验。
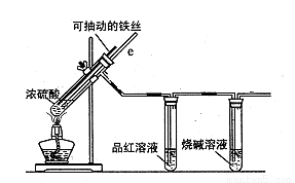
(1)写出铁与浓硫酸反应的化学方程式 ;
若在取用浓硫酸的过程中,不慎在皮肤上沾少量浓硫酸,处理的方法是 。
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻止SO2气体逸出而防止污染环境;二是 。
(3)品红溶液的作用是 。
(4)小组讨论后认为:由于常用的铁丝是铁碳合金,生成的气体中还可能含有CO2。写出生成CO2的化学方程式 。
查看答案和解析>>
科目: 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:填空题
某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
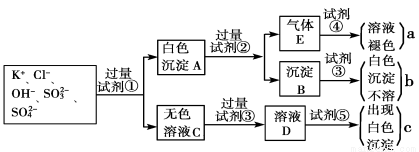
请回答下列问题:
(1)白色沉淀A与试剂②反应的离子方程式是__________________________________。
(2)无色溶液C中加入试剂③的主要目的是____________________________________。
(3)试验中若只加试剂③而不加试剂②,对实验的影响是_______________________。
(4)气体E通入试剂④发生反应的离子方程式是__________________________________。
查看答案和解析>>
科目: 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:计算题
有一硫酸和硝酸的混合溶液,取出20mL,加入足量BaCl2溶液,经过滤、洗涤、烘干后得沉淀9.32g;滤液与4.0mol/L的氢氧化钠溶液35mL恰好完全中和。试求:
(1)原混合溶液中硫酸和硝酸的物质的量浓度。
(2)另取10mL原溶液,加入0.96g铜粉共热,生成一氧化氮的体积为多少?
(3)另取10mL原溶液,加入1.92g铜粉共热,,至少还要向反应后的溶液中加入多少毫升1mol/L硫酸才能将铜粉恰好完全溶解?
查看答案和解析>>
科目: 来源:2013-2014四川省眉山市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是
A.医药中常用酒精消毒是因为酒精能够使细菌蛋白体发生盐析
B.开发清洁能源汽车(如太阳能汽车等)能减少或控制汽车尾气污染
C.目前废旧电池的回收,主要是为了防止电池中NH4Cl对水资源的污染
D.为了防止中秋月饼等富脂食品氧化变质,可在包装袋中放入生石灰
查看答案和解析>>
科目: 来源:2013-2014四川省眉山市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.水玻璃长时间放置在空气中:SiO32-+CO2+H2O=H2SiO3↓+HCO3-
B.硫酸铜溶液显酸性:Cu2++2H2O=Cu(OH)2↓+2H+
C.用石墨电极电解饱和食盐水:2H++2Cl-  H2↑+Cl2↑
H2↑+Cl2↑
D.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com