
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在pH=1的溶液中:K+、Na+、SO42–、HCO3-
B.在0.1 mol·L-1 Na2CO3溶液中:Al3+、K+、NO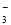 、SO42–
、SO42–
C.在0.1 mol·L-1 FeCl3溶液中:K+、NH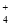 、I-、SCN-
、I-、SCN-
D.在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO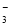
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
在常温下四个容积相同的抽空的密闭容器内,分别注入下列各组气体(先注入一种,再注入另一种),全部气体注入完毕后,容器中的压强从大到小的顺序是
①2mol氢气和1mol氧气 ②2mol硫化氢和1mol二氧化硫
③2mol一氧化氮和1mol氧气 ④2mol氨和lmol氯化氢
A.①=②=③>④ B.①>②=③>④ C.③>④>①>② D.①>③>④>②
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
在A2+3B2 = 2C的反应中,经过t秒钟后,C的浓度增加了0.6mol/L,在此期间,反应速率V(B2)=0.45mol/(L·S),则t值为
A.1秒 B.1.5秒 C.2秒 D.2.5秒
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
下列有关原子结构和元素周期律表述正确的是
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
分类是化学研究的重要方法之一,下列有关说法中,正确的是
A.SO2、NO2、和CO2都属于酸性氧化物
B.甲烷和和一氯甲烷都属于烷烃
C.HC1O是弱电解质,NaClO却属于强电解质
D.在水溶液中能电离出H+的化合物都属于酸
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3﹑H2O﹑Cl2、H+ 、Cl-和Co2+ 。下列叙述不正确的是
A.氧化产物为Cl2
B.氧化剂与还原剂的物质的量之比为1∶2
C.若有3mol H2O生成,则反应中有2mol电子转移
D.当该反应生成2.24L Cl2时,则反应中有0.1mol电子转移
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
已知下列反应的热化学方程式为:
(1)C(s)+O2(g)=CO2(g) ΔH 1=-393.5kJ/mol
(2)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH 2=-870.3kJ/mol
(3)H2(g)+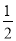 O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
则2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的反应热ΔH为
A.+488.3 kJ/mol B.-488.3 kJ/mol C.-244.15 kJ/mol D.+244.15 kJ/mol
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. | B. | C. | D. |
通电一段时间后,搅拌均匀,溶液的pH增大 | 甲电极上的电极反应为: 2Cl- -2e- = Cl2↑ | Pt电极上的电极反应为:O2+2H2O+4e-==4OH- | 总反应的离子方程式为: 2Fe3++Cu=Cu2++ 2Fe2+ |
|
|
|
|
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为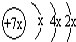 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为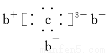 ,下列比较中正确的是( )
,下列比较中正确的是( )
A.原子半径:a>c>d>b B.最高价氧化物对应水化物的酸性:c>d>a
C.原子序数:a>d>b>c D.单质的氧化性:a>b>d>c
查看答案和解析>>
科目: 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
某实验小组依据反应 设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是

A.调节pH可以改变反应的方向
B.pH = 0.68时,反应处于平衡状态
C.pH = 5时,负极电极反应式为2I--2e- =I2
D.pH >0.68时,氧化性I2〉AsO43-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com