
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
写出下列物质的电子式,有结构式的请写出结构式
①氨气 、 ②氯化铵 、
③干冰 、 ④苛性钠 、
⑤冰 、 ⑥过氧化钠 、
⑦双氧水 、 ⑧HClO 、
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时到达平衡,依图所示:
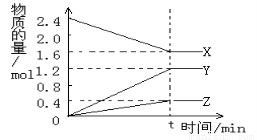
①该反应的化学方程式是 。
②反应起始至t,Y的平均反应速率是 。
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
一定条件下,可逆反应:A2+B2  2C达到平衡。经测定,平衡时c(A2)=0.5mol/L,c(B2)=0.1mol/L,c(C)=1.6mol/L,若A2、B2和C的起始浓度分别为amol/L,bmol/L,cmol/L。
2C达到平衡。经测定,平衡时c(A2)=0.5mol/L,c(B2)=0.1mol/L,c(C)=1.6mol/L,若A2、B2和C的起始浓度分别为amol/L,bmol/L,cmol/L。
请回答:
(1)a、b应满足的关系是 (2)a的取值范围是
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:简答题
以色列科学家达尼埃尔·谢赫特曼因发现“准晶体”而独享2011年诺贝尔化学奖以及奖金。现在,准晶体已在很多应用领域“大展拳脚”,可用来制造不粘锅、发光二极管、热电转化设备等。
(1)铁在周期表中的位置 ,铝的原子结构示意图为 ;
(2)工业炼铝用的原料是 (填Al2O3或AlCl3),不用另一种的原因是
;
(3)铜在潮湿的空气中会生成铜绿,写出该反应方程式
;
(4)用电解法制Fe(OH)2沉淀,下列可做电解质溶液的是
A.纯净水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
在恒温时,向某密闭容器中通入2mol X和1mol Y气体,发生如下反应:
2X(气)+Y(气) 2Z(气),压强一定时,测得在平衡时Z的体积分数为0.4。
2Z(气),压强一定时,测得在平衡时Z的体积分数为0.4。
(1)与上述平衡保持同温、同压,若向密闭容器中通入4mol X(气)、2mol Y(气),达到平衡,则Z的体积分数为 ;平衡时,气体的总物质的量是 。
(2)若向密闭器中通入X(气)和Y(气)的物质的量分别记为n(X)、n(Y),保持容器容积不变,并满足平衡时Z的体积分数为0.4,则n(X)/n(Y)的取值范围为 。
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:简答题
在恒温、恒压和使用催化剂的条件下,已知:在容积可变的密闭容器中,充入1 L含3 mol H2和1 mol N2的混合气体,反应达平衡时有a mol NH3生成,N2的转化率为b%。
(1)若在恒温、恒压和使用催化剂的条件下,在体积可变的密闭容器中充入x mol H2和y mol N2,反应达平衡时有3a mol NH3生成,N2的转化率仍为b%。则x= ;
y= 。
(2)在恒温、恒压和使用催化剂的条件下,设在体积可变的密闭容器中充入x mol H2、y mol N2和z mol NH3,若达平衡时N2转化率仍为b%,则x、y的关系为 ;z的取值范围为 。
(3)在恒温[与(1)温度相同]和使用催化剂的条件下,在容积不可变的密闭容器中,充入1 L含3 mol H2和1 mol N2的混合气体,反应达平衡时N2的转化率为c%,则b、c的关系为 (用“<”、“=”或“>”表示),理由是 。
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
(1)下列四种粒子中,半径按由大到小的排列顺序是 。
①基态X的原子结构示意图:○+16
②基态Y的价电子排布式:3s23p5
③基态Z2-的电子排布图:
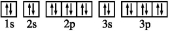
④W基态原子有2个能层,电子式:∶∶
(2)已知An+、B(n+1)+、Cn-、D(n+1)-都具有相同的电子层结构,则A、B、C、D的原子半径由大到小的顺序是 ,离子半径由大到小的顺序是 ,原子序数由大到小的顺序是 。
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
加热时,N2O5可按下列分【解析】
N2O5  N2O3 + O2,N2O3又可按下列分【解析】
N2O3 + O2,N2O3又可按下列分【解析】
N2O3  N2O + O2。今将 4 molN2O5充入一升密闭容器中,加热至 t℃时反应达到了平衡状态。平衡时,c(O2)= 4.5 mol/L, c(N2O3)= 1.62 mol/L,c(N2O)= mol/L,此时N2O5的分解率为 。
N2O + O2。今将 4 molN2O5充入一升密闭容器中,加热至 t℃时反应达到了平衡状态。平衡时,c(O2)= 4.5 mol/L, c(N2O3)= 1.62 mol/L,c(N2O)= mol/L,此时N2O5的分解率为 。
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:推断题
请仔细阅读以下转化关系:
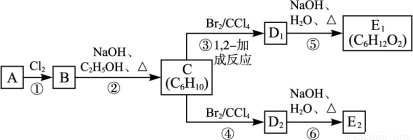
已知:(ⅰ)烃类化合物A的质谱图表明其相对分子质量为84;红外光谱表明其分子中含有碳碳双键;核磁共振氢谱显示其分子中只有一种氢原子。(ⅱ)D1、D2互为同分异构体,E1、E2互为同分异构体。
请结合以上信息回答下列问题:
(1)A的结构简式为 。A分子中的碳原子是否都处于同一平面? (填“是”或“不是”)。
(2)写出反应②的化学方程式: 。
(3)写出下列反应的反应类型:
反应② 、反应④ 、反应⑥ 。
(4)写出E1的结构简式并用系统命名法给C命名:
E1 ,C的名称: 。
(5)化合物F是A的同系物,相对分子质量为56,写出F所有可能的结构: 。
(6)写出在加热和浓硫酸作用下,E2与足量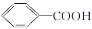 反应的化学方程式: 。
反应的化学方程式: 。
查看答案和解析>>
科目: 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
A、B、C、D、E是五种短周期元素,原子序数依次增大。前四种的原子序数之和是E的原子序数的二倍。E的阳离子与D的阴离子都比A阳离子多2个电子层。D与四种元素中任意一种都可形成原子个数比不相同的若干种化合物。B是形成化合物种类最多的元素。请回答下列问题:
(1)写出元素符号:A________,E________。
(2)D在周期表中位于第_______周期第________族。
(3)五种元素原子半径由大到小的顺序是(用A~E字母表示)_______________。
(4)A、B、C、D可形成一种受热易分解的化合物,写出该化合物受热分解的化学方程式____________________________________________________________。
(5)A、B、D可形成A2B2D4型化合物,该化合物的名称是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com