
科目: 来源:2013-2014北京市西城区高三二模理综化学试卷(解析版) 题型:选择题
在2 L的密闭容器中进行如下反应: CO(g)+H2O(g) CO2(g)+H2(g),有如下数据:
CO2(g)+H2(g),有如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
CO | H2O | CO2 | H2 | CO2 | ||
1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
下列说法正确的是
A.正反应为吸热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K=8/3
D.实验1再加入1.0 mol H2O,重新达到平衡时,n (CO2)为1.6 mol
查看答案和解析>>
科目: 来源:2013-2014北京市西城区高三二模理综化学试卷(解析版) 题型:推断题
(17分)
铃兰醛具有甜润的百合香味,常用作肥皂、洗涤剂和化妆品的香料。合成铃兰醛的路线如下图所示(部分试剂和条件未注明):
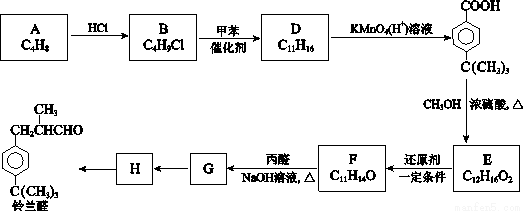
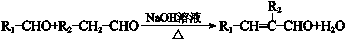
已知:i.
ii.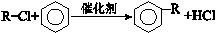
请回答:
(1)由A生成B的反应类型是 。
(2)D的结构简式是 。
(3)生成E的化学方程式是 。
(4) F 能发生银镜反应,F的结构简式是 。
(5)下列有关G的叙述中,不正确的是 。
a.G分子中有4种不同化学环境的氢原子
b.G能发生加聚反应、氧化反应和还原反应
c.1 mol G最多能与4 mol H2发生加成反应
(6)由H生成铃兰醛的化学方程式是 。
(7)F向G转化的过程中,常伴有分子式为C17H22O的副产物K产生。K的结构简式是 。
(8)以有机物A、苯酚、甲醛及必要的无机物为原料合成某高分子树脂,
其结构为  ,合成路线是 。
,合成路线是 。
示例: 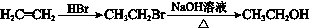
查看答案和解析>>
科目: 来源:2013-2014北京市西城区高三二模理综化学试卷(解析版) 题型:简答题
(13分)
海水是巨大的化学资源宝库。
Ⅰ.从海水中可以提取氯、溴、碘等卤族元素。
(1)Cl2的电子式是 。
(2)已知:X2 (g)+H2(g) 2HX(g) (X2表示Cl2、Br2和I2)。
2HX(g) (X2表示Cl2、Br2和I2)。
下图表示平衡常数K与温度t的关系。

①ΔH 表示X2与H2反应的焓变,ΔH 0。(填“>”、“<”或“=”)
② 曲线a表示的是 (填“Cl2”、“Br2”或“I2”)与H2反应时K与t的关系。
Ⅱ.海水淡化具有广泛的应用前景,淡化前需对海水进行预处理。
(1)通常用明矾[K2SO4·Al2(SO4)3·24H2O]作混凝剂,降低浊度。明矾水解的离子方程式是 。
(2)用下图所示NaClO的发生装置对海水进行消毒和灭藻处理。

① 装置中由NaCl转化为NaClO的化学方程式是 。
② 海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3。生成CaCO3的离子方程式是 。
③ 若每隔5-10 min倒换一次电极电性,可有效地解决阴极的结垢问题。
试用电极反应式并结合必要的文字进行解释 。
查看答案和解析>>
科目: 来源:2013-2014北京市西城区高三二模理综化学试卷(解析版) 题型:实验题
(13分)
利用某含铬废液[含较低浓度的Na2Cr2O7、Fe2(SO4)3]制备K2Cr2O7。
流程如下:
Ⅰ.用NaOH溶液调pH至3.6,产生红褐色沉淀,过滤;
Ⅱ.向滤液中加入Na2SO3,一定操作后分离出Na2SO4;
Ⅲ.将分离出Na2SO4后的溶液调pH约为5,得到Cr(OH)3沉淀;
Ⅳ.在KOH存在条件下,向Cr(OH)3中加入足量H2O2溶液,得到黄色溶液;
Ⅴ.向黄色溶液中加入物质A后,溶液变为橙红色,一定操作后得到K2Cr2O7固体;
Ⅵ.测定K2Cr2O7固体的纯度。
已知:Cr2O72-(橙红色)+H2O 2CrO42-(黄色)+2H+
2CrO42-(黄色)+2H+
(1)步骤Ⅰ中红褐色沉淀的化学式是 。
(2)步骤Ⅱ中加入Na2SO3的目的是 。
(3)步骤Ⅳ中反应的离子方程式是 。
(4)步骤Ⅴ中加入的物质A可以是 。(填序号)
a.KOH b.K2CO3 c.H2SO4 d.SO2
(5)步骤Ⅵ的操作是:取0.45 g K2Cr2O7产品配成溶液,酸化后滴入18.00 mL
0.50 mol/L的FeSO4溶液,恰好使Cr2O72-完全转化为Cr3+。产品中K2Cr2O7的纯度是 。(注:K2Cr2O7的摩尔质量为294 g/mol)
(6)向橙红色的K2Cr2O7溶液中,滴加Ba(NO3)2溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是 ,溶液pH变小的原因是 。
查看答案和解析>>
科目: 来源:2013-2014北京市西城区高三二模理综化学试卷(解析版) 题型:简答题
(15分)
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。
Ⅰ.化合物SO2Cl2中S元素的化合价是 。
Ⅱ.用二氧化锰和浓盐酸制氯气的化学方程式是 。
Ⅲ.在收集氯气前,应依次通过盛有饱和食盐水和 的洗气瓶。
Ⅳ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体,
充分反应后,将液体和剩余气体分离,进行如下研究。

(1)研究反应的产物。向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。
① 写出SO2Cl2与H2O反应的化学方程式 。
② 检验该溶液中Cl-的方法是 。
(2)继续研究反应进行的程度。用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。
① 该白色沉淀的成分是 。
② 写出SO2与Cl2反应的化学方程式,并阐述理由______。
查看答案和解析>>
科目: 来源:2013-2014北京市通州区高考二模理综化学试卷(解析版) 题型:选择题
下列说法中,正确的是
A.气象环境报告中新增的“PM2.5”是对一种新分子的描述
B.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关
C.小苏打是制作面包等糕点的膨松剂,苏打是治疗胃酸过多的一种药剂
D.乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的
查看答案和解析>>
科目: 来源:2013-2014北京市通州区高考二模理综化学试卷(解析版) 题型:选择题
用下列装置进行相应实验,能达到实验目的的是
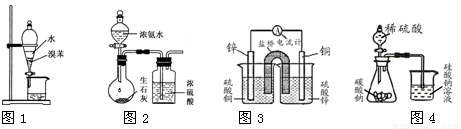
A.用图1所示装置分离出溴苯
B.用图2 所示装置制取干燥的氨气
C.用图3设计成铜锌原电池装置
D.用图4证明氢化物稳定性SiH4>CH4>H2S
查看答案和解析>>
科目: 来源:2013-2014北京市通州区高考二模理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.氨气通入醋酸溶液:CH3COOH+NH3=CH3COONH4
B.亚硫酸氢钠溶液呈酸性:HSO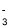 +H2O
+H2O H3O++SO
H3O++SO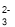
C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
D.稀硝酸洗涤试管内壁的银镜:Ag+2H++NO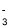 =Ag++NO↑+H2O
=Ag++NO↑+H2O
查看答案和解析>>
科目: 来源:2013-2014北京市通州区高考二模理综化学试卷(解析版) 题型:选择题
下列有关化学概念或原理的论述中,正确的是
A.任何一个氧化还原反应都可以设计为电池,输出电能
B.铅蓄电池放电时的负极和充电时的阴极均发生氧化反应
C.电解饱和食盐水的过程中,水的电离平衡正向移动
D.任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大
查看答案和解析>>
科目: 来源:2013-2014北京市通州区高考二模理综化学试卷(解析版) 题型:选择题
已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说
法正确的是
X | Y |
Z | W |
A.若四种元素均为非金属,则W的最高价氧化物对应的水化物一定是强酸
B.若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
C.若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
D.若四种元素中只有一种为金属,则Z与Y的最高价氧化物对应的水化物能反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com