
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
常温下,以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+等,通过添加过量的难溶电解质MnS,可使这些金属离子形成硫化物沉淀并过滤除去,下列说法正确的是
A.过滤后的溶液中一定没有S2-
B.MnS难溶于水,可溶于MnCl2溶液中
C.常温时,CuS、PbS、CdS比MnS更难溶
D.加入MnS后生成CuS的离子方程式是Cu2+ + S2- = CuS↓
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
在恒温恒容密闭容器中进行的合成氨反应,下列选项一定能作为达到平衡状态标志的是
A.混合气体的密度不再发生变化
B.反应过程中v(N2):v(H2)=1:3
C.反应过程中c(N2):c(H2):c(NH3)=1:3:2
D.单位时间内断开a mol H-H键的同时断开2a mol N-H键
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.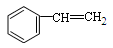 没有顺反异构体
没有顺反异构体
B.1,3-丁二烯可以作为合成高分子化合物的原料
C.用乙醇和浓硫酸制备乙烯时,用水浴加热控制反应温度
D.常温下,将苯酚加入到少量水中有浑浊,滴入适量NaOH溶液后浑浊消失
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
关于苹果酸(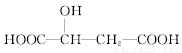 )说法正确的是
)说法正确的是
A.苹果酸不易溶于水而易溶于有机溶剂
B.和苹果酸具有相同官能团的同分异构体只有1种
C.1 mol苹果酸与足量NaOH溶液反应时,最多消耗3 mol NaOH
D.1mol苹果酸与足量NaHCO3溶液反应时,最多可得44.8LCO2(标准状况下)
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
下列叙述的理由与结论因果关系正确的是
选项 | 理由 | 结论 |
A | 与盐酸反应时,相同物质的量的原子失去电子的数目:Al>Na | 还原性:Al>Na |
B | 室温时,相同物质的量浓度溶液的pH:AlCl3<MgCl2 | 碱性:Mg(OH)2>Al(OH)3 |
C | 相同数目的分子可电离的H+数:H2SO4>HClO4 | 酸性:H2SO4>HClO4 |
D | 用饱和NaHCO3溶液可以除去CO2 中含有的少量SO2 | 非金属性:S > C |
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
下图是模拟工业电解饱和食盐水的装置图,
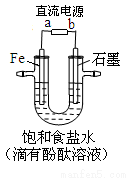
下列叙述不正确的是
A.a为电源的负极
B.Fe电极的电极反应是4OH――4e-= 2H2O+O2↑
C.通电一段时间后,铁电极附近溶液先变红
D.电解饱和食盐水的化学方程式是2NaCl + 2H2O 2NaOH + H2↑+ Cl2↑
2NaOH + H2↑+ Cl2↑
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属元素,且与R同周期。下列叙述不正确的是
A.离子半径大小:Y2- > M2- > R3+
B.Z与M组成的某种化合物能形成酸雨
C.Y与M组成的化合物跟水反应后一定能得强酸
D.X、Y、R的最高价氧化物的水化物两两之间能发生反应
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
甲、乙两物质的溶解度曲线如图所示,下列说法正确的是

A.t1℃时,物质的量浓度:甲=乙
B.温度变化相同时,溶解度数值的变化量:甲>乙
C.t2℃时,饱和溶液中溶质的质量分数:甲=乙
D.相同质量的饱和溶液由t2℃降到t1℃时,析出的固体:甲<乙
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:
2N2O5(g)  4NO2 (g)+ O2(g) ΔH > 0t℃时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2 (g)+ O2(g) ΔH > 0t℃时,向密闭容器中通入N2O5,部分实验数据见下表:
时间/s | 0 | 500 | 100 0 | 150 0 |
c(N2O5)/ mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法中不正确的是
A.500 s 内N2O5分解速率为2.96╳10-3mol·L-1·s-1
B.达平衡时,N2O5的转化率为50%
C.达平衡后,升高温度平衡常数减小
D.达平衡后,其他条件不变,将容器的体积压缩到原来的一半,c(N2O5)> 5.00 mol·L-1
查看答案和解析>>
科目: 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
下列选项中的原因或结论与现象不对应的是
选项 | 现象 | 原因或结论 |
A | 在 H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
B | 向5mL 0.005mol·L-1FeCl3溶液中加入5mL 0.015mol·L-1KSCN溶液,溶液呈红色,再滴加几滴1mol·L-1KSCN溶液,溶液颜色加深 | 增大反应物浓度,平衡向正反应方向移动 |
C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 该反应△H<0,平衡向生成NO2方向移动 |
D | 在密闭容器中有反应:A+xB(g) | A非气体、x=1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com