
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
下列实验“操作和现象”与“目的或结论”对应关系正确的是
| 操作和现象 | 目的或结论 |
A | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
B | 向铁和稀硝酸反应后的溶液中若滴加KSCN溶液显红色;若滴加酸性高锰酸钾溶液紫红色褪去 | 该溶液中既有Fe3+,还有Fe2+ |
C | 将铁插入硫酸铜溶液中 | 比较Cu、Fe2+的还原性 |
D | 将产生的气体依次通过无水CuSO4、澄清石灰水和品红溶液 | 检验碳与浓硫酸反应后的气体产物 |
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列表示气体X组成的选项中合理的是
A.0.3 mol NO、0.1 mol NO2
B.0.3 mol NO2、0.1 mol NO
C.0.6 mol NO
D.0.3 mol NO2
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
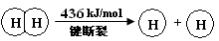

下列说法不正确的是
A.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
B.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
C.破坏1 mol H—O 键需要的能量是463.4 kJ
D.H2(g) + 1/2O2(g)=H2O(l) ΔH <-241.8 kJ/mol
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
下列解释事实或实验现象的化学用语正确的是
A.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O 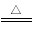 Fe(OH)3↓+ 3H+
Fe(OH)3↓+ 3H+
B.酸性KI淀粉溶液久置后变蓝4I-+O2+2H2O=2I2+4OH-
C.实验室盛装NaOH溶液的试剂瓶不能用玻璃塞 SiO2 +2OH- = SiO32-+H2O
D.钢铁表面的水膜酸性较强时,水膜中的H+会被还原O2+4H++4e- = 2H2O
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
下列图示与对应的叙述一定正确的是
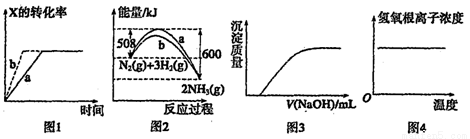
A.图1所示反应:X(g)+Y(g) 2Z(g),b的压强一定比a大
2Z(g),b的压强一定比a大
B.图2表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂
C.图3表示向Ca(HCO3)2溶液中滴入NaOH溶液所得沉淀的质量变化
D.图4表示明矾溶液受热时氢氧根浓度随温度的变化
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
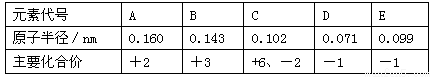
A.A、B的单质与稀盐酸反应速率B>A
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
铝是一种很重要的金属,可以发生一系列反应制备物质。

下列说法错误的是
A.反应①又称铝热反应,曾用于野外焊接铁轨
B.利用反应②③都能产生氢气,且产生等量氢气消耗Al的质量和转移电子数分别相等
C.反应①②中铝均作还原剂
D.常用反应⑥制备Al(OH)3,方法是向Al2(SO4)3溶液中滴加NaOH溶液至恰好完全沉淀
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
根据表中信息判断,下列选项不正确的是
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO4- | Cl2、Mn2+ |
A.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
B.第①组反应的氧化产物为O2
C.第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
D.第③组反应中生成1mol Cl2,转移电子2mol
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:填空题
(本小题14分)现有A、B、C、D四种短周期主族元素,其原子序数依次增大。已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。请回答下列问题:
(1)元素D在周期表中的位置是________________________。
(2)C2B2所含的化学键类型有___________;请写出C2B2与A2B反应的离子方程式________________。
(3)元素B、C形成的简单离子中半径较大的是_________(写电子式)。
(4)仅由C、D两种元素组成的一种盐溶于水后pH>7的原因是_____________ (用离子方程式表示)。
(5)如图所示以铂作电极,以C、D两元素的最高价氧化物的水化物X、Y的溶液作为电解质溶液,A、B元素的单质分别在两电极上发生原电池反应,则通入B单质的电极反应式为_________,通入A单质的X溶液的pH将__________(填“增大”、“不变”或“减小”)。
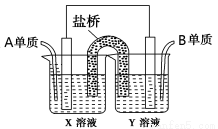
查看答案和解析>>
科目: 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:填空题
(本小题14分)氮气是制备含氮化合物的一种重要物质,而含氮化合物的用途广泛。
(1)图中表示两个常见的固氮反应:
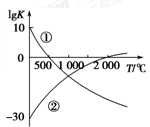
①N2+3H2 2NH3
2NH3
②N2+O2 2NO的平衡常数(lg K)与温度的关系,
2NO的平衡常数(lg K)与温度的关系,
根据图中的数据判断下列说法正确的是________(填序号)。
A.反应②为放热反应
B.常温下,反应①的反应速率很大,而反应②的反应速率很小
C.升高温度,反应①的反应速率增大,反应②的反应速率减小
D.在常温下,利用反应①固氮和利用反应②固氮反应程度相差很大
(2)工业上也可在碱性溶液中通过电解的方法实现由N2制取NH3:2N2+6H2O 4NH3+3O2,通入N2的一极是________(填“阴极”或“阳极”),阳极的电极反应式是____ ____。
4NH3+3O2,通入N2的一极是________(填“阴极”或“阳极”),阳极的电极反应式是____ ____。
(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应:
①N2(g)+3H2O(l) 2NH3(g)+
2NH3(g)+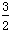 O2(g) ΔH=a kJ/mol。
O2(g) ΔH=a kJ/mol。
已知:②N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol,
2NH3(g) ΔH=-92.4 kJ/mol,
2H2(g)+O2(g) 2H2O(l) ΔH=-571.6 kJ/mol,则a=__________。
2H2O(l) ΔH=-571.6 kJ/mol,则a=__________。
(4)已知:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=-1316 kJ·mol-1 ,氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。
2N2(g)+6H2O(g) ΔH=-1316 kJ·mol-1 ,氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。
①当温度不同(T2>T1)、其他条件相同时,下列图像正确的是________(填代号)。
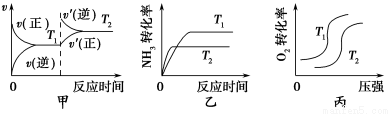
②该燃料电池的负极反应式是____________________________________。
(5)工业上合成氨时,温度过高,氨气的产率降低,试从化学平衡移动原理的角度加以解释:__________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com