
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:选择题
高温下2HBr(g) H2(g)+Br2(g); △H>0,达到平衡时,要使混合气体颜色加深,可采取的方法
H2(g)+Br2(g); △H>0,达到平衡时,要使混合气体颜色加深,可采取的方法
A.升高温度 B.降低温度 C.减小压强 D.增大H2浓度
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:选择题
决定化学反应速率的最主要因素是
A.温度和压强 B.反应物的浓度
C.参加反应的各物质的性质 D.催化剂的加入
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:选择题
可逆反应: 2NO2(g)  2NO(g)+O2(g),在容积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在容积固定的密闭容器中,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦ C.①③④⑤ D.①②③④⑤⑥⑦
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:选择题
在一定温度不同压强(P1<P2)下,可逆反应2A(g)  2B(g) + C(g)中,生成物C在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
2B(g) + C(g)中,生成物C在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
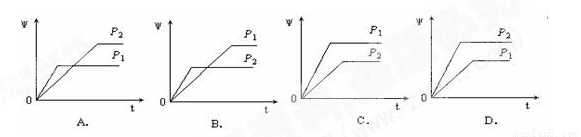
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:选择题
将1L含有0.4molCuSO4和0.2molNaCl的水溶液用惰性电极电解,电解一段时间后,在一个电极上得到0.3molCu,另一个电极上产生气体(标况)的体积是
A.4.48L B.5.6L C.6.72L D.13.44L
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:选择题
对已达化学平衡的下列反应 2X(g)+Y(g) 2Z(g),减小压强时,对反应产生的影响是
2Z(g),减小压强时,对反应产生的影响是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都增大,平衡向正反应方向移动
D.正、逆反应速率都减小,平衡向逆反应方向移动
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:填空题
(6分)在一定体积的密闭容器中,进行如下化学反应:
C(s)+H2O(g)  CO(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
t/(℃) | 700 | 800 | 830 | 1000 | 1200 |
K | 0.7 | 0.8 | 1.0 | 1.6 | 2.4 |
(1)该反应的化学平衡常数表达式为K=____ ____,该反应为________反应(填“吸热”或“放热”)。
(2)能作为判断反应达到化学平衡状态的依据是________。
A.容器中压强不变 B.c(H20)不变
C.v正(H2)=v逆(H2O) D.c(H2)=c(CO)
(3)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,缩小容器的体积,平衡________移动(填“正向”、“逆向”或“不”)。H2O(g)的浓度___ ____,CO(g)的浓度___ ____(填“变大”、“不变”或“变小”)
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:填空题
(16分)如图为相互串联的甲乙两个电解池,
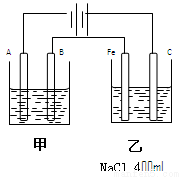
请回答:
(1)甲池若为电解精炼铜的装置,A极是 ,材料是 ,电极反应为 ,B极是 ,材料是 ,电极反应为 。
(2)若甲槽阴极增重12.8g,则乙槽阴极放出气体在标准状况下的体积为 。
(3)若乙槽剩余液体为400mL,求电解后得到碱液的物质的量浓度 。
查看答案和解析>>
科目: 来源:2014秋安徽省高二上学期期中化学试卷(解析版) 题型:填空题
(8分)氨气主要用作致冷剂及制取铵盐和氨肥
(1)某研究小组在673K、30MPa条件下,在体积为VL的密闭容器中进行反应:N2(g)+3H2(g)? 2NH3(g),其n(H2)和n(NH3)随时间变化的关系如图所示.
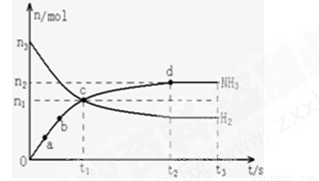
下列叙述正确的是 .
A.点a的正反应速率比点b的大
B.点c处反应达到化学平衡状态
C.若t3时由673K升至773K,则n(H2)将增大
D.t2、t3时刻,n(N2)不相等
(2)在一定温度和催化剂下,将6.4mol H2和2.4molN2混合于一个容积为4L的密闭容器中发生反应,在3min末时反应恰好达平衡,此时生成了1.6mol NH3.①3min内以H2表示的化学反应速率 ;②该条件下的平衡常数
(3)已知:N2(g)+O2(g)=2NO(g)△H= +180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H= -92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H= -483.6kJ/mol
写出氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com