
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
下列说法正确的是
A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
下列关于铜电极的叙述不正确的是
A.铜锌原电池中铜是正极
B.用电解法精炼铜时粗铜作阳极
C.在镀件上镀铜时可用铜作阳极
D.电解稀硫酸溶液制H2、O2时铜做阳极
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
在一个定容密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下反应生成NH3,10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
A.0.1 mol·L-1·min-1 B.0.3 mol·L-1·min-1
C.0.2 mol·L-1·min-1 D.0.6 mol·L-1·min-1
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
已知:2Zn(s)+O2(g)=2ZnO(s) ΔH= -701.0kJ·mol-1
2Hg(l)+O2(g)=2HgO(s) ΔH= -181.6kJ·mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l)的ΔH为
A.+519.4kJ·mol-1 B.+259.7 kJ·mol-1
C.-259.7 kJ·mol-1 D.-519.4kJ·mol-1
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
在N2 (g)+ 3H2(g) 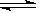 2 NH3 (g)的平衡体系中,其他条件不变,增加氮气的浓度,下列判断正确的是
2 NH3 (g)的平衡体系中,其他条件不变,增加氮气的浓度,下列判断正确的是
A.氮气的转化率增大
B.氢气的转化率增大
C.氨气在平衡混合气体中的百分含量一定增大
D.氨气的分解速率大于氨气的生成速率
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
一定条件下,对于可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c
2Z(g),若X、Y、Z的起始浓度分别为c 、c
、c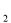 、c
、c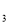 (均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是
(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是
A.c :c
:c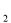 =1:2
=1:2
B.平衡时,Y和Z的生成速率之比为2:3
C.X、Y的转化率相等
D.c 的取值范围为0.04 mol/L<c
的取值范围为0.04 mol/L<c <0.14 mol/L
<0.14 mol/L
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
在298K时,2SO2(g)+O2(g)  2SO3(g) ΔH=-197 kJ·mol-1 ,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1; 向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2,则下列关系中正确的是
2SO3(g) ΔH=-197 kJ·mol-1 ,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1; 向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2,则下列关系中正确的是
A.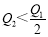 B.
B.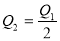 C.
C.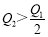 D.
D.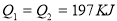
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应:2R(g)+5Q(g)
4X(g)+nY(g)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是
A.2 B.3 C.4 D.5
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
下列各装置中都盛有0.1 mol·L—1 的NaCl溶液,放置一定时间后,锌片的腐蚀速率由快到慢的顺序是
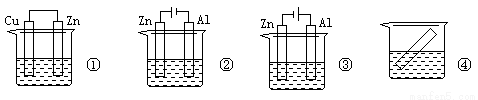
A.③①④② B.①②④③ C.①②③④ D.②①④③
查看答案和解析>>
科目: 来源:2014秋安徽省宿州市高二上学期期中化学(理)试卷(解析版) 题型:选择题
对于某温度下平衡体系mA(g) + nB(g) pC(g) + qD(g) △H<0,下列说法不正确的是
pC(g) + qD(g) △H<0,下列说法不正确的是
A.若温度不变将容器容积扩大到原来的2倍,此时A的浓度变为原来的0.52倍,则m + n > p + q
B.向平衡体系中加入C、D,该反应的△H减小
C.若温度和容器体积不变,充入一定量的惰性气体,B的浓度不变
D.若平衡时,增加A的量,A的转化率下降,B的转化率增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com