
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:填空题
(10分)为了证明醋酸是弱电解质,甲、乙、丙、丁、戊分别选用下列试剂进行实验: 0.1mol/L醋酸溶液、0.1mol/L盐酸、C(H+)=10-3mol/L的盐酸、C(H+)=10-3mol/L的醋酸、CH3COONa晶体、石蕊试液、pH试纸、锌粒、蒸馏水。已知:pH=-lgc(H+)
(1)甲用pH试纸测出0.10mol/L的醋酸溶液pH=4,则认定醋酸是弱电解质,你认为这一方法 (填“正确”或“不正确”)。
(2)乙分别取用10ml 0.1mol/L盐酸和醋酸,然后加入完全一样的等量锌粒(少量),产生氢气用气球收集,通过观察实验现象为 ,则认定醋酸是弱电解质。
(3)丙取出10ml0.10mol/L醋酸溶液,滴入石蕊试液,显红色,再加入醋酸钠晶体,颜色变浅红色,也能证明醋酸是弱电解质,试从电离平衡原理解释 。
(4)丁分别取用10ml C(H+)=10-3mol/L盐酸和醋酸,然后加入完全一样的等量锌粒(足量),产生氢气用气球收集,通过比较产生气球的大小,如果醋酸产生气球 (填“大”或“小”),则认定醋酸是弱电解质。
(5)戊取用C(H+)=10-3mol/L的醋酸稀释到原来的100倍,稀释后醋酸的C(H+) 10-5mol/L
(填“>”、“<”、“=”),则认定醋酸是弱电解质。
查看答案和解析>>
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:填空题
(16分) 已知2A2(g)+B2(g) 2C3(g);△H =-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ。
2C3(g);△H =-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ。
(1)比较a b(填“>、=、<”)
(2)若将反应温度升高到700℃,该反应的平衡常数将 (填“增大”“减小”或“不变”)。若将反应容器的体积压缩,平衡向 方向移动(填“正反应”或”逆反应”),该反应的平衡常数将 。(填“增大”“减小”或“不变”)
(3)若在原来的容器中,只加入2 mol C3,500 ℃时充分反应达平衡后,吸收热量ckJ,C3的浓度也是w mol/L,则c 等于 (用a、b表示)。
(4)能说明该反应已经达到平衡状态的是
A 2v逆(A2)=v正(B2) B v正(C3)=2v正(B2)
C A2与C3浓度相等 D.混合气体的平均相对分子质量不变
E.容器内压强保持不变 F.容器内密度保持不变
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
(6)若将上述容器改为恒压容器(反应前体积相同),起始时加入2 mol A2和1molB2,500 ℃时充分反应达平衡后,放出热量dkJ,则d b(填“>、=、<”)
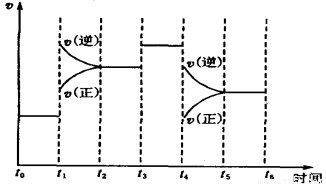
(7)下图表示此反应的反应速率v和时间t的关系图。
根据下图判断,在t1和t4时刻改变的外界条件分别是 和 。
查看答案和解析>>
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:填空题
(10分) 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=a kJ·mol-1,测得CO2和CO浓度随时间的变化如图所示:
FeO(s)+CO(g) ΔH=a kJ·mol-1,测得CO2和CO浓度随时间的变化如图所示:
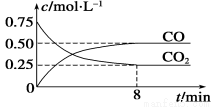
(1) 0~8 min,v(CO)=__________mol·L-1·min-1。
(2) 测得在不同温度下,K值如下:
温度(℃) | 500 | 700 |
平衡常数K | 2.00 | 2.50 |
①若500℃时进行反应,CO2起始浓度为3 mol·L-1,CO的平衡浓度为________。
②反应中的a________0(填“大于、小于、等于”)。
③下列措施中,能使平衡时c(CO)/c(CO2)的比值的增大的是________(填序号)。
A.升高温度 B.再加入一些铁粉 C.增大压强 D.充入一定量氮气
④在700℃时的某时刻测得CO2浓度为1.4mol·L-1,CO浓度为2.0mol·L-1,反应向 方向进行(填“正反应”或”逆反应”),理由是: 。
查看答案和解析>>
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:填空题
(20分)
(1)已知可逆反应:M(g)+N(g)P(g)+Q(g) ΔH>0,请回答下列问题:
①在某温度下,反应物的起始浓度分别为:c(M)= 1 mol·L-1,c(N)=2.4 mol·L-1,达到平衡后,M的转化率为60%,此时N的转化率为 ;
②若反应温度不变,反应物的起始浓度分别为:c(M)=4 mol·L-1,c(N)=a mol·L-1;达到平衡后,c(P)=2 mol·L-1,a= ;
(2)甲、乙两瓶氨水的浓度分别为1 mol·L-1和0.1 mol·L-1,则甲、乙两瓶氨水中c(OH-)之比_______(填“大于”、“小于”或“等于”)10,说明理由_____________________________ 。
(3)25℃时几种物质的电离度(溶液浓度均为0.1mol/L) 如下表(已知硫酸的第一步电离是完全的):
①H2SO4溶液: HSO4- | ②NaHSO4溶液: HSO4- | ③盐酸 HCl=H++Cl |
10% | 29% | 100% |
25℃时,0.1mol/L上述几种溶液加入完全一样的等量锌粒,反应速率从大到小的顺序
是 (填序号)
②25℃时,c(H+)相同的上述几种溶液,其物质的量浓度由大到小的顺序是 (填序号)
③25℃时,0.1mol/L H2SO4中的HSO4-的电离度小于0.1mol/L NaHSO4中HSO4-的电离度的原因是________________ 。
查看答案和解析>>
科目: 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
以“改革驱动,走向生态文明新世代”为主题的生态文明贵阳国际论坛2014年7月在贵阳召开,本次年会确定以植树造林增加碳汇的方式,实现“碳中和”目标。下列行为与此次目标不相符的是
A.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,以提高空气质量
B.开发时能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料
C.大力开采煤、石油和天然气,以满足经济发展的需要
D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放
查看答案和解析>>
科目: 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
近两年来,“雾霾”一直是人们所关注的对象,下图为雾霾的主要成分示意图。下列说法不正确的是( )
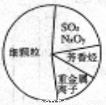
A.SO2和NxOy溶于水均只生成酸
B.重金属离子可导致蛋白质变性
C.苯是最简单的芳香烃
D.大量燃烧化石燃料时造成雾霾天气的一种重要因素
查看答案和解析>>
科目: 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
俄罗斯科学家用铪和钨两种核素精确确定了地球和月球的年龄,得出月球至少比地球早700万年形成。它们是根据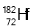 和
和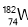 两种核素的含量比例得出的。下列有关
两种核素的含量比例得出的。下列有关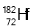 和
和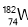 关系的说法正确的是
关系的说法正确的是
A.中子数相等 B.原子质量几乎相同
C.互为同位素 D.在周期表中处于相邻位置
查看答案和解析>>
科目: 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
当光束通过下列分散系,能观察到丁达尔现象的是( )
① 有尘埃的空气 ②稀盐酸 ③蒸馏水 ④墨水
A.②③ B.①④ C.③④ D.① ②③④
查看答案和解析>>
科目: 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
下列关于C、Si、Ge、Sn、Pb的比较,正确的是( )
A.它们的最外层电子数随核电荷数增加而增多
B.它们的最高价氧化物均可溶于水生成相应的酸
C.它们单质的氧化性随核电荷数的增加而逐渐减弱
D.它们的氢化物的稳定性随核电荷数的增加而逐渐增强
查看答案和解析>>
科目: 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
下列关于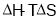 说法中正确的是( )
说法中正确的是( )
A.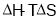 可用于判断所有条件下的反应能否自发进行
可用于判断所有条件下的反应能否自发进行
B.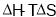 只用于判断温度、体积一定的反应能否自发进行
只用于判断温度、体积一定的反应能否自发进行
C.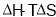 只用于判断温度、压强一定的反应能否自发进行
只用于判断温度、压强一定的反应能否自发进行
D.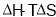 <0的反应,在该条件下一定剧烈反应
<0的反应,在该条件下一定剧烈反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com