
科目: 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入350 mL 2 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24 L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为
A.0.21 mol B.0.25 mol C.0.3 mol D.0.35 mol
查看答案和解析>>
科目: 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I-、NO3-、CO32-、SO42-、AlO2-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈酸性,可以排除__________的存在。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4呈紫红色,可以排除____ __的存在。
(3)另取出部分溶液逐滴加入NaOH溶液,使溶液由酸性逐渐变为碱性,反应过程中均无沉淀产生,则又可排除________的存在。
(4)取出部分(3)中的碱性溶液加入Na2CO3溶液,有白色沉淀生成,证明有________的存在,可以排除_____的存在。
查看答案和解析>>
科目: 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
2011年3月,日本发生9级地震,地震引发海啸及伤亡。灾区重建面临多种困难,其中饮水安全是重要问题之一。高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如下方案制备高铁酸钾:
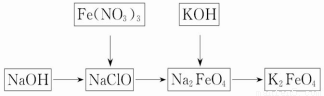
(1)高铁酸钾中铁元素的化合价为_______价,推测它具有的化学性质是____ __。
(2)在次氯酸钠(NaClO,84消毒液的主要成分)溶液中加入烧碱固体形成碱性环境,将研磨的硝酸铁少量多次地加入到上述溶液中,冰浴中反应1h。发生的离子反应为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,氧化剂是________。将KOH加入到反应后的溶液搅拌半小时。静置,抽滤粗产品。该反应的化学方程式为2KOH+Na2FeO4====K2FeO4+2NaOH。根据复分解反应原理,高铁酸钠的溶解度________高铁酸钾的溶解度(填“大于”、“小于”或“等于”)。
(3)在强碱性溶液中,高铁酸钾能将亚铬酸盐(KCrO2)氧化为铬酸盐(K2CrO4),生成的铬酸盐溶液酸化后,得到的重铬酸钾(K2Cr2O7)用Fe(Ⅱ)的标准溶液滴定,以二苯胺磺酸钠为指示剂。到达滴定终点时,溶液由紫色变为淡绿色(+6价铬转化成+3价铬)。有关离子方程式为FeO42-+CrO2-+2H2O====CrO42-+Fe(OH)3↓+OH-,2CrO42-+2H+====Cr2O72-+H2O,Cr2O72-+6Fe2++14H+====2Cr3++6Fe3++7H2O
现称取5.00 g高铁酸钾样品于烧杯中,加入适量氢氧化钾溶液,加入稍过量的KCrO2,充分反应后,转移到250 mL容量瓶中,定容,量取25.00 mL,再用稀硫酸酸化,用0.100 0 mol·L-1的(NH4)2Fe(SO4)2标准溶液滴定,用去标准溶液30.00 mL。计算上述实验制得的样品中,高铁酸钾的质量分数为__________;
查看答案和解析>>
科目: 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:(已知:硅不与盐酸和水反应)
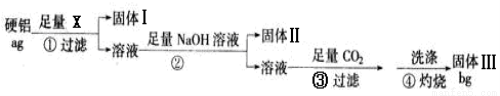
(1)若固体Ⅰ中含有铜和硅,步骤①的试剂X应选择 (填“NaOH溶液”,“盐酸”,“FeCl3溶液”);步骤②的操作是 ,反应的离子方程式为 , 。
(2)固体Ⅲ的化学式为 步骤④反应的化学方程式为 。
(3)步骤④中的沉淀没有用蒸馏水洗涤时,会使测定结果 (填“偏高”“偏低”“不影响”)
查看答案和解析>>
科目: 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P亚层中有4个电子。
(1)D原子的电子排布式为 ,若A元素的原子最外层电子排布为1s1,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于 键。
(2)当n=2时,B的原子结构示意图为 ,B与C形成的晶体属于 晶体。
当n=3时,B与C形成的晶体属于 晶体。
(3)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,元素A在周期表中的位置是 ,A、B、C、D四种元素的电负性由大到小的顺序是 (用元素符号表示)。
(4)C和D的最简单氢化物相比较:稳定性: (填化学式,下同);
沸点: 原因是 。
查看答案和解析>>
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列叙述中,不能用勒夏特列原理解释的是 ( )
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成SO3的反应
C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D.实验室用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列有关说法正确的是 ( )
A.活化分子的总数越多,反应速率越快
B.升高温度,活化分子百分数不变,活化分子数增多,化学反应速率增大
C.使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率增大
D.加入反应物,使活化分子百分数增大,化学反应速率增大
查看答案和解析>>
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
可逆反应A+3B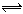 2C+2D,在4种不同情况下的反应速率分别为单位mol·Lˉ1·sˉ1:
2C+2D,在4种不同情况下的反应速率分别为单位mol·Lˉ1·sˉ1:
①VA=0.20;②VB=0.60 ;③VD=0.50;④ VC=0.45;该反应速率最快的是 ( )
A.② B.③ C.①和④ D.②和③
查看答案和解析>>
科目: 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列情况下,反应速率相同的是 ( )
A.等体积0.1 mol/L HCl和0.1 mol/L H2SO4分别与0.2 mol/L NaOH溶液反应
B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应
C.等体积等浓度HCl和HNO3分别与等质量的Na2CO3粉末反应
D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com