
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
将铝、铁物质的量均为0.2mol的某种铝铁合金粉末分别于下列溶液充分反应(溶液均过量),放出氢气最多的是
A.18.4mol·L-1H2SO4溶液
B.1.5mol·L-1 HCl溶液
C.4mol·L-1 HNO3溶液
D.3mol·L-1 NaOH溶液
查看答案和解析>>
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
现将1mo1Cu2S与144克FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2 、CuSO4的混合溶液,并产生NO气体。则最终消耗的硝酸的物质的量是
A.12mo1 B.15mo1 C.16mo1 D.17mo1
查看答案和解析>>
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200 mL c(OH-)= 0.1mol/L的溶液,然后逐滴加入1 mol/L 的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,

则下列说法正确的是
A.原合金质量为 0.92 g
B.图中V2为 100
C.整个加入盐酸过程中 Na+的浓度保持不变
D.Q点m1为0.78
查看答案和解析>>
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的净化处理。某工厂欲以工业废料(金属铁、铝及其氧化物)为原料、采用如下流程来制取PAFC:
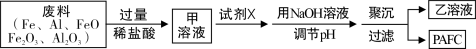
下列判断无法确定的是
A.PAFC因水解而能净水
B.往甲溶液中滴入KSCN溶液后呈血红色
C.试剂X具有氧化性
D.乙溶液肯定不可能呈强碱性
查看答案和解析>>
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:填空题
(16分)X、Y、Z、W四种常见元素,且均为短周期元素。
已知:①X的最高价氧化物对应的水化物为无机酸中最强酸
②Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料
③Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料
④W被称为军事金属,可在CO2中燃烧。
(1)X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为 。
(2)Z的氧化物在通讯领域用来作 ,工业上制Z单质的化学反应方程式为 。
(3)在50mL ,lmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积最多为 mL。
(4)Y、W合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某Y、W合金(设不含其他元素)中W的质量分数,设计下列三种不同的实验方案进行探究。填写下列空白:
[探究一]
实验方案:Y、W合金 测定剩余固体质量
测定剩余固体质量
实验步骤:
①称取一定质量的Y、W合金粉末样品,加入过量的Na0H溶液,充分反应。实验中发生反应的化学方程式是 。
②过滤、洗涤、干燥、称量剩余固体。若未洗涤固体,将导致测得的W的质量分数
(填“偏高”或“偏低”)。
[探究二]
实验方案:称量xg Y、W合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧。

问题讨论:
③欲计算W的质量分数。该实验中还需测定的数据是 。
④若用空气代替O2进行实验,对测定结果是否有影响? (填“是”或“否”)。
查看答案和解析>>
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:填空题
(7分)向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式__________________________________________;
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至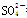 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用右图中的曲线表示是________(填序号).
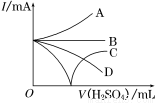
查看答案和解析>>
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:实验题
(15分)某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验室按以下步骤进行:
①称量a g样品,置于烧杯中;
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全;
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤、洗涤沉淀;
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量;
请根据上面叙述,回答:
(1)下图所示仪器中,本实验步骤①②③中必须用到的仪器是E和 (填字母)。
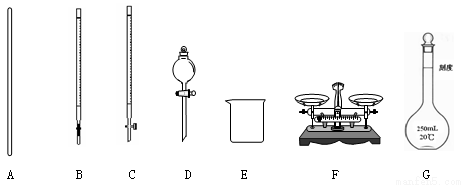
(2)写出步骤③中发生反应的离子方程式 。
(3)洗涤是洗去附着在沉淀上的 (写离子符号),洗涤沉淀的操作是 。
(4)如何确定沉淀是否洗涤干净的操作是 。
(5)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为 。(列出算式,不需化简)
(6)该兴趣小组中甲学生认为:实验步骤③中不加入氯水,其余步骤不变,仍可达到实验目的。你认为甲学生的观点是否正确? (填正确或错误);请说明理由: 。
查看答案和解析>>
科目: 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:实验题
(14分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
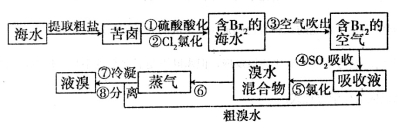
(1)步骤①中用硫酸酸化的目的是____________________________________________。
步骤②发生反应的离子方程式为_____________________________________________。
(2)步骤④利用了SO2的还原性,反应的离子方程式为___________________________。
(3)操作⑥的名称是________________。
(4)从含溴海水中吹出的溴也可用纯碱吸收。纯碱吸收溴的主要反应是:Na2CO3+Br2→NaBrO3+NaBr+CO2,吸收1molBr2时,转移的电子数为________mol。纯碱吸收后再用硫酸酸化,单质溴又从溶液中析出。
(5)化学上将SCN 、OCN
、OCN 、CN
、CN 等离子称为“类卤离子”。现将KSCN溶液滴加到酸性Fe3+溶液中,溶液立即变成血红色;通入SO2后,血红色消失。血红色消失过程中发生反应的离子方程式为______________________________________。
等离子称为“类卤离子”。现将KSCN溶液滴加到酸性Fe3+溶液中,溶液立即变成血红色;通入SO2后,血红色消失。血红色消失过程中发生反应的离子方程式为______________________________________。
查看答案和解析>>
科目: 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:选择题
下列现象或变化过程与胶体的性质无关的是 ( )
A.清晨森林中的道道光柱 B.夕阳下的晚霞
C.海水的淡化 D.明矾净水
查看答案和解析>>
科目: 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:选择题
下列有关实验的叙述正确的是( )
A.将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液
B.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH
C.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应
D.读取滴定管内液体的体积,俯视读数导致读数偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com