
科目: 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
已知KCl、K2Cr2O7、CrCl3、Cl2 、HCl在溶液中可以形成一个氧化还原反应体系。
(1)已知反应中有水生成,则反应物分别是K2Cr2O7和 (填化学式),当电子转移数为6mol时,化学方程式中水的化学计量数是 。
(2)反应过程中,被还原的元素是_________。
查看答案和解析>>
科目: 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
下表为元素周期表的一部分。请参照元素①~⑧在表中的位置,回答下列问题:

(1)④⑤⑥的原子半径由小到大的顺序为(用元素符号表示) 。
②③⑦的最高价含氧酸的酸性由弱到强的顺序是(用化学式表示) 。
(2)④与⑤常温下可发生反应生成化合物A,请用电子式表示A的形成过程______________。
(3)由表中元素①③④⑥⑧所形成的常见物质X、Y、Z、M、N可发生以下反应:

①X溶液与Y溶液反应的离子方程式为 ;
②由N制取⑥对应的单质所采用的方法是 ;
③M溶液呈酸性,原因是(用离子方程式解释) 。
查看答案和解析>>
科目: 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
(1)P4(s,白磷)+5O2(g)=2P2O5(s)△H =-2983.2kJ/mol
P(s,红磷)+5/4O2(g)=1/4P4O10(s)△H =-738.5kJ/mol
则相同的状况下,能量较低的是______;白磷的稳定性比红磷______(填“高”或“低”)。
(2)CH3—CH3 (g)→ CH2=CH2(g)+H2(g);有关化学键的键能如下。
化学键 C-H C=C C-C H-H
键能(kJ/mol) 414 615 347 435
试计算该反应的反应热为__________.
查看答案和解析>>
科目: 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
如下图是一个乙醇燃料电池工作示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
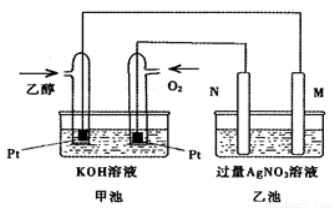
(1)M电极材料是 , N的电极反应式为 ,加入乙醇的铂电极的电极反应式为 。
(2)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出约为30kJ热量,表示乙醇燃烧热的热化学方程式为 。
(3)若M、N均为石墨电极,将乙池改为电解500mL含KNO3和Cu(NO3)2的混合液一段时间后,在两极上均生成11.2L(标准状况)气体。则M极产生的气体是H2,原混合液中Cu2+的物质的量浓度是 mol/L。
查看答案和解析>>
科目: 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
有机物A、B、C、D、E、F、G、H相互转化关系如下图所示。5.2 g F能与100 mL 1 mol/L NaOH溶液恰好完全中和,0.1 mol F还能与足量NaHCO3反应,在标准状况下放出4.48 L CO2。D的分子式为C3H3O2Na,E的分子中含有羧基。
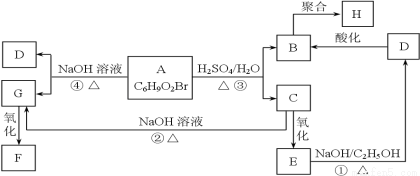
(1)写出物质C中的官能团的名称: ;
(2)写出物质F、H的结构简式;
F 、H ;
(3)写出反应①、④的化学反应类型:① 、④ ;
(4)写出变化①的化学方程式
(5)写出相对分子质量比B大14,且与B具有相同官能团的物质的结构简式(仅写一种)。
。
查看答案和解析>>
科目: 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:

已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用。
②ClO2气体在中性和碱性溶液中不能稳定存在。
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式 。
(2)反应生成ClO2气体需要X酸酸化,X酸可以为 。
A.盐酸 B.稀硫酸 C.HI溶液
(3)吸收塔内的温度不能过高的原因为 。
(4)ClO2被S2-还原为ClO2-、Cl-转化率与pH关系如图。

写出pH≤2时ClO2与S2-反应的离子方程式: 。
查看答案和解析>>
科目: 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
温度(℃) | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①写出工业合成氨的化学方程式 。
②由上表数据可知该反应为放热反应,理由是 。
③理论上,为了增大平衡时H2的转化率,可采取的措施是 。(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应 CH4(g) + H2O (g) CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的 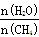 恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
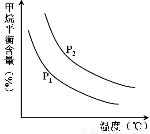
①图中,两条曲线表示压强的关系是:P1 P2(填“>”、“=”或“<”)。
②该反应为 反应(填“吸热”或“放热”)。
(3)原料气H2还可通过反应CO(g) + H2O(g)  CO2 (g) + H2(g) 获取。
CO2 (g) + H2(g) 获取。
①T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为 ,该反应平衡常数的表达式为 。
②保持温度仍为T ℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是 (填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n (CO) : n (H2O) : n (CO2) : n (H2) = 1 : 1 : 1 : 1
查看答案和解析>>
科目: 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列各组物质,前者是混合物,后者是纯净物的是
A.水玻璃 玻璃 B.石油 盐酸
C.干冰 铝热剂 D.氯水 液氯
查看答案和解析>>
科目: 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.可用丁达尔现象区分溶液与胶体
B.化学变化能够实现一种原子变为另一种原子
C.O3是由3个氧原子构成的化合物
D.CuSO4?5H2O是一种混合物
查看答案和解析>>
科目: 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列化合物中,只能在水溶液中才能导电的电解质是
A.NaCl B.H2SO4 C.NH3 D.CaO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com