
科目: 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:选择题
Fenton试剂常用于氧化降解有机污染物X。在一定条件下,反应初始时c(X)=2.0×10-3 mol·L-1,反应10 min进行测定,得图1和图2。下列说法不正确的是
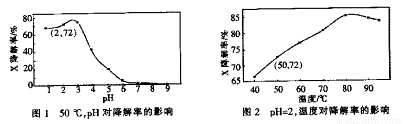
A.50oC,PH在3~6之间,X降解率随pH增大而减小
B.pH=2,温度在40~80 oC,X降解率随温度升高而增大
C.无需再进行后续实验,就可以判断最佳反应条件是:PH=3、温度为80 oC
D.pH=2、温度为50oC,10min内v(X)=1.44x10-4mol·L-1min-1
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:计算题
(共12分)
(1)Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液。
①该Ba(OH)2溶液的物质的量浓度为___________________;
②溶液中由水电离出c(OH―)=______________;
③该浓度Ba(OH)2溶液与某浓度盐酸溶液按体积比1∶9混合后,所得溶液pH=11(忽略体积的变化),该盐酸溶液的pH=____________。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数KW=_____________。该温度___________25℃(填“>”“=”或“<”)。
(3)常温下,将1 mL pH=1的H2SO4溶液加水稀释至100mL,稀释后的溶液中
c(H+)/ c(OH-)=_______________。
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:填空题
(14分)
(1)某课外兴趣小组用下图装置进行实验,
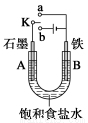
试回答:
①若开始时开关K与a连接,则A电极反应式为____________________。
②若开始时开关K与b连接,则A电极反应式为____________________。
③若开始时开关K与b连接,电路中通过0.2 NA个电子时,两极共产生 ____________mol气体
④若开关K与b连接,铁和石墨棒互换位置,描述U型管中观察到的现象:_____ _ 。
(2)如下图所示的装置,C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答以下问题:
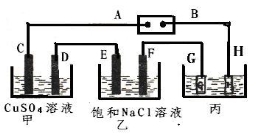
①B是电源的 _极
②甲装置中D电极的电极反应式: _____________________________ 。
③欲用丙装置给铜镀银,G应该是 _ (填“银”或“铜”),电镀液的主要成分是(填化学式) 。
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:实验题
(10分)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10mL2% H2O2溶液 | 无 |
② | 10mL5% H2O2溶液 | 无 |
③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_____________________________________。
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。


分析上图能够得出的实验结论是______________________________________。
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:填空题
(16分)碳及其化合物应用广泛。
I 工业上利用CO和水蒸汽反应制氢气,存在以下平衡:
CO(g)+H2O(g)  CO2(g)+H2(g) △H>0
CO2(g)+H2(g) △H>0
(1)向1L恒容密闭容器中注入CO(g)和H2O(g),830℃时测得部分数据如下表。则该温度下反应的平衡常数K=______________。
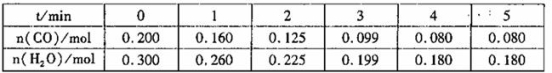
(2)相同条件下,向1L恒容密闭容器中,同时注入2mol CO、2mol H2O(g),1molCO2和1mo1H2,此时v(正 ) __________v(逆)(填“>”“=”或“<”)
(3)上述反应达到平衡时,要提高CO的转化率,可采取的措施是_______(填字母代号)。
A.升高温度
B.加入催化剂
C.增大压强
D.增加CO的浓度
E.及时分离出CO2
II 已知CO(g)+1/2 O2 (g)=CO2 (g) △H=一141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=一484 kJ·mol-1
CH3OH(1)+3/2O2 (g)=CO2(g)+2H2O(g) △H=一726 kJ·mol-1
(4)用CO(g)、H2(g)化合制得液态甲醇的热化学方程式为___________________________。
III某同学设计了一个甲醇燃料电池,并用该电池电解100mL一定浓度NaCl与CuSO4混合溶液,其装置如图:

(5)写出甲中通入甲醇这一极的电极反应式__________________________________ 。
(6)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式____________,原混合溶液中CuSO4的物质的量浓度____________mol/L。(假设溶液体积不变)
(7)将在t2时所得的溶液稀释至200mL,该溶液的pH约为___________。
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是(NA表示阿伏加德罗常数的值)
A.在常温常压下,11.2 L N2含有的分子数为0.5NA
B.在常温常压下,2g H2含有的原子数为2NA
C.在标准状况下,18 g H2O的体积约为22.4 L
D.0.1mol/L NaCl溶液中所含的Na+数为0.1 NA
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列关于物质的保存不正确的是
A.钠保存在煤油中 B.氯水保存棕色细口瓶中
C.液氯可以保存在干燥的钢瓶中 D.溴化银保存在无色试剂瓶中
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列物质对应的用途错误的是
A.镁合金:航空、航天材料 B.小苏打:焙制糕点的发酵粉
C.明矾:消毒、杀菌作用 D.过氧化钠:漂白剂和供氧剂
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
在4份碘化钾淀粉溶液中,分别加入下列物质,不能使溶液变蓝的是
A.氯水 B.溴水 C.碘水 D.碘化钠溶液
查看答案和解析>>
科目: 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
海带中含碘元素,从海带中提取碘有如下步骤:①通入足量Cl2;②将海带焙烧成灰后加水搅 拌;③加CCl4振荡;④用分液漏斗分液;⑤过滤。则合理的操作顺序是
A.①②③④⑤ B.②⑤①③④
C.①③⑤②④ D.②①③⑤④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com