
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
已知碳有三种常见的同位素:12C、13C、14C,氧也有三种同位素:16O、17O、18O,由这六种微粒构成的二氧化碳分子(O=C=O)中,其相对分子质量最多有
A.7种 B.8种 C.6种 D.12种
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
下列物质中按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是
A.F2、K、HCl B.Cl2、Al、H2
C.NO2、Na、Br2 D.O2、SO2、H2O
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
研究表明:多种海产品如虾、蟹、牡蛎等,体内含有+5价的砷(As)元素,但它对人体是无毒的,砒霜的成分是As2O3,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜+大量维生素C=砒霜。下面有关解释不正确的是
A.维生素C能将+5价砷氧化成As2O3
B.维生素C具有还原性
C.青菜中含有维生素C
D.使人中毒的过程中砷元素发生还原反应
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见下图)。下列说法正确的是
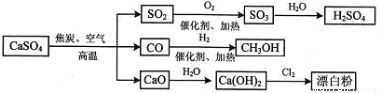
A.CO、SO2、SO3均是酸性氧化物
B.除去与水反应的两个反应,图示其余转化反应均为氧化还原反应
C.工业上利用Cl2和澄清石灰水反应来制取漂白粉
D.漂白粉的成分为Ca(ClO)2
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
从1897年英国首次使用氯气对给水管网消毒以来,氯气用于自来水消毒已经经历了100多年的历史。目前,我国大多数城市仍然采用氯气消毒法对自来水进行净化、消毒。氯气之所以长期用于自来水消毒,原因是
A.氯气有毒,可以毒死细菌、病毒
B.氯气具有刺激性气味,可以熏死细菌、病毒
C.氯气与水反应生成的HClO,可以杀死水中的细菌、病毒
D.氯气用于自来水消毒的工艺简单、成熟,易于操作,且成本低
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
在氯水中存在多种分子和离子可通过实验的方法加以确定,下列说法中可能错误的是
A.加入含有NaOH的酚酞试液,红色褪去,说明有H+存在
B.加入有色布条后,有色布条褪色,说明有HClO分子存在
C.氯水呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在
D.加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
对于加热条件下反应3Cl2+6KOH = 5KCl+KClO3+3H2O,以下叙述正确的是
A.Cl2是氧化剂,KOH是还原剂
B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1
C.Cl2既是氧化剂又是还原剂
D.每生成1mol的KClO3转移6mol的电子
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:填空题
下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
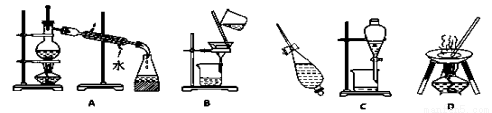
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)分离植物油和水________________;
(2)除去粗盐中的泥沙_________________;
(3)与海水晒盐原理相似的是______ _;
(4)用四氯化碳在碘水中提取碘_________;
(5)分离CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合物(互溶)______;
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:填空题
对一份稀溶液作初步分析发现,溶液无色、澄清,其中可能含有SO42-、Na+、CO32- 、H+、NO3-、NH4+、Cl-等离子中的若干种。然后又做了如下实验,以确认这些离子是否大量存在。
①用pH试纸测溶液的pH,试纸显红色;
②取2毫升溶液,用氯化钡和稀硝酸进行检验,结果生成了白色沉淀;
③对②中所得混合物充分静置后,取上层清夜用硝酸银溶液和稀硝酸检验,结果又生成了白色沉淀;
④另取2毫升溶液,加入足量氢氧化钠溶液并加热,没有产生能使湿润红色石蕊试纸变蓝的气体。
试回答下述问题:
(1)原溶液中一定存在的离子是
(2)原溶液中一定不存在的离子是
(3)按上述操作,原溶液中还不能肯定是否存在的阳离子是
检验该阳离子方法是
查看答案和解析>>
科目: 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:实验题
实验室需要0.5 mol·L-1硫酸溶液450 mL。可供选择的仪器有:
①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧分液漏斗
实验室现有质量分数为98%、密度为1.84 g·cm-3的浓H2SO4提供,根据这种溶液的配制情况回答下列问题:
(1)上述仪器中,一直用不到的有 (填序号)。
(2)下列操作中,容量瓶不具备的功能有______________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.作为反应容器
(3)配制时应量取浓硫酸_________mL。
(4)实验中,玻璃棒的作用有____________________________________。
(5)配制溶液时,下列操作中引起误差偏高的有________________。(填序号)
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,仰视标线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com