
科目: 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向浓度为0.1mol/LNaCl、KI混合液中逐滴加入AgNO3溶液 | 出现黄色沉淀 | 溶解性:AgCl>AgI |
| B | 溴乙烷与NaOH的乙醇溶液共热,将溢出气体通入酸性高锰酸钾溶液中 | 溶液紫色褪去 | 证明有乙烯生成 |
| C | 向X的溶液中滴入浓NaOH溶液,将干燥红色石蕊试纸置于管口 | 无明显现象 | X溶液中有NH4+ |
| D | 将SO2气体通入Ba(NO3)2溶液 | 产生白色沉淀 | 沉淀为BaSO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目: 来源: 题型:

| 金属离子 | 开始沉淀时的pH | 沉淀完全的pH |
| Al3+ | 3.4 | 4.7 |
| Cu2+ | 4.1 | 6.9 |
| Mg2+ | 9.4 | 12.4 |
查看答案和解析>>
科目: 来源: 题型:



| 滴定次数 | 第一次 | 第二次 | 第三次 |
| 滴定前读数(mL) | 0.10 | 0.36 | 1.10 |
| 滴定滴定后读数(mL) | 20.12 | 20.34 | 22.12 |
查看答案和解析>>
科目: 来源: 题型:
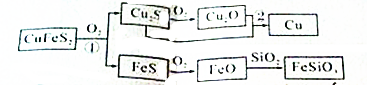
查看答案和解析>>
科目: 来源: 题型:
 已知草酸为二元弱酸:
已知草酸为二元弱酸:| A、pH=1.2溶液中:c(K+)+c(H+)=c(OH-)+c(H2C2O4) |
| B、pH=2.7溶液中:c2(HC2O4-)/[c(H2C2O4)×c(C2O42-)]=1000 |
| C、将相同物质的量KHC2O4和K2C2O4固体完全溶于水可配得pH为4.2的混合液 |
| D、向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离度一直增大 |
查看答案和解析>>
科目: 来源: 题型:

| TiCl4 | SiCl2 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| 顺序 | 步骤 | 实验现象 |
| ① | 取少量纯净的NaCl,加适量蒸馏水溶解 | 溶液无变化 |
| ② | 滴入少量淀粉-KI溶液,振荡 | 溶液无变化 |
| ③ | 然后再滴加稀硫酸,振荡 | 溶液变蓝色 |
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量食盐样品于试管中,加适量蒸馏水使其完全溶解, | |
| 步骤2:另取少量食盐样品于试管中,加适量蒸馏水使其完全溶解,滴入适量的稀硫酸酸化, |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com