
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、1 mol[Zn(NH3)4]Cl2中含有σ键的数目为16NA |
| B、电解精炼粗铜时,每转移NA电子,阳极上溶解的铜原子数必为0.5NA |
| C、3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1NA |
| D、60 g石英晶体中含有的Si-O键数目为2NA |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、分馏、蒸馏、煤的液化都是物理变化,干馏、裂化、裂解都是化学变化 |
| B、乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 |
| C、需要加热的反应不一定是吸热反应 |
| D、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| A、放出热量关系:a<b<196 |
| B、三个容器内反应的平衡常数:③>①>② |
| C、达平衡时SO3的体积分数:③>① |
| D、SO2的转化率:②>①>③ |
查看答案和解析>>
科目: 来源: 题型:
 向甲、乙、丙三个密闭容器中充入一定量的X和Y,发生反应:x(g)+aY(g)═2Z(g).各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以如图和下表表示.下列说法不正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的X和Y,发生反应:x(g)+aY(g)═2Z(g).各容器的反应温度、反应物起始量,反应过程中Z的浓度随时间变化关系分别以如图和下表表示.下列说法不正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.0molX 0.5molY | 1.0molX 0.5molY | 4.0molX 2.0molY |
| A、该反应温度升高,平衡常数减小 |
| B、20min内甲容器中反应的平均速率:v(X)=0.075mol?(L?min)-1 |
| C、其他条件不变,若缩小乙的体积,Y的转化率不变 |
| D、10min时,其他条件不变,向乙容器中再加入2 molZ,平衡向逆反应方向移动 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| A、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| B、煤经过气化和液化等物理变化可以转化为清洁燃料 |
| C、多糖、油脂、蛋白质均能发生水解反应 |
| D、浸泡过高锰酸钾溶液的硅藻土可以吸收乙烯,所以可用此物保鲜水果 |
查看答案和解析>>
科目: 来源: 题型:
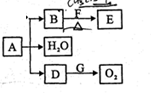 (Ⅰ)已知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应能与NaOH溶液反应,试回答下列问题:
(Ⅰ)已知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应能与NaOH溶液反应,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com