
科目: 来源: 题型:
| A、用高锰酸钾溶液滴定Na2SO3溶液至终点:滴入最后一滴高锰酸钾溶液,溶液恰好由紫色变为无色,且半分钟不变色 |
| B、通常用产生气泡的快慢,比较不同条件下Na2S2O3溶液与稀硫酸反应速率 |
| C、润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从下口放出,重复2~3次 |
| D、制备硫酸亚铁晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液被全部蒸干 |
查看答案和解析>>
科目: 来源: 题型:
| 0.01mol?L-1KIO3酸性溶液的体积/mL | 0.01mol?L-1KI溶液的体积/mL | H2O的体积 /mL | 实验温度/℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | 5 | 5 | 25 | t1 |
| 实验2 | 4 | 5 | V1 | 25 | t2 |
| 实验3 | 5 | 5 | 5 | 35 | t3 |

查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| 实验序号 | a | b | c |
| 合金质量(g) | 0.51 | 0.765 | 0.918 |
| 气体体积(mL) | 560 | 672 | 672 |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 5 |

查看答案和解析>>
科目: 来源: 题型:
| A、蛋白质和油脂都是天然高分子化合物 |
| B、石油的裂化和煤的干馏,都属于化学变化 |
| C、等质量的葡萄糖和果糖在人体内完全氧化释放的能量相等 |
| D、聚氯乙烯制品易造成白色污染,可采用焚烧处理 |
查看答案和解析>>
科目: 来源: 题型:
3 2 |
4 2 |
3 2 |
4 2 |
A、
| ||||
B、
| ||||
C、
| ||||
D、32He原子核内含有3个质子,
|
查看答案和解析>>
科目: 来源: 题型:
A、 |
| B、CH2=CH2+Cl2+Ca(OH)2→CH2-CH2+CaCl2+H2O |
C、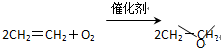 |
D、 |
查看答案和解析>>
科目: 来源: 题型:
4 2 |
56 28 |
132 50 |
208 82 |
16 8 |
17 8 |
18 8 |
298 114 |
298 114 |
289 114 |
查看答案和解析>>
科目: 来源: 题型:
| A、lH、2H、3H为同素异形体 |
| B、lH、2H、3H的中子数相同 |
| C、lH、2H、3H互为同位素 |
| D、lH、2H、3H的质量数相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com