
科目: 来源: 题型:
| A、5.0L | B、8.9L |
| C、15.7L | D、26.9L |
查看答案和解析>>
科目: 来源: 题型:
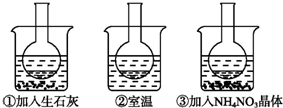 如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.
如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.查看答案和解析>>
科目: 来源: 题型:
| A、K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 |
| B、NaCl、Na2CO3、NaOH三者饱和溶液的pH逐渐变大 |
| C、NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低 |
| D、金、银、铜金属活动性顺序逐渐减弱 |
查看答案和解析>>
科目: 来源: 题型:
| A、用润湿的pH试纸测稀碱溶液的pH,测定值偏小 |
| B、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C、滴定前滴定管内无气泡,终点读数时有气泡,所取体积偏小 |
| D、锥形瓶用待测液润洗,所测溶液浓度偏大 |
查看答案和解析>>
科目: 来源: 题型:
| A、一定含有Ag+ |
| B、一定含有SO42- |
| C、一定含有Ag+或SO42- |
| D、一定含有SO32-或SO42- |
查看答案和解析>>
科目: 来源: 题型:
| A、水的屯离程度:①<② |
| B、①、②中粒子浓度关系均符合:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(co32-) |
| C、向③、④中分别加入25 mL 0.l mol?L-1盐酸后,溶液中c(NH4+):③<④ |
| D、将③、④混合,所得溶液的pH>7,则该溶液中:c(NH4+)=c(NH3?H2O) |
查看答案和解析>>
科目: 来源: 题型:
| A、Na+、Ca2+、Cl-、SO42- |
| B、Fe2+、H+、SO32-、ClO- |
| C、Mg2+、NH4+、Cl-、SO42- |
| D、K+、Fe3+、NO3-、SCN- |
查看答案和解析>>
科目: 来源: 题型:
| A、Ba2+ NO3- NH4+ |
| B、Na+ K+ SO32- |
| C、Ca2+ CO32- Cl- |
| D、ClO- Na+ NH4+ |
查看答案和解析>>
科目: 来源: 题型:
| A、无色透明溶液中:Ca2+、H+、Cl-、Fe2+ |
| B、能与金属铝反应发出氢气的溶液:K+、NO3-、Cl-、Fe3+ |
| C、由水电离出的c(H+)=1.0×10-12mol/L的溶液:Na+、Cu2+、HCO3-、NO3- |
| D、KW/c(H+)=0.1mol/L的溶液中:Na+、K+、CO32-、NO3- |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com