
科目: 来源: 题型:
| A、pH=6的某溶液 |
| B、加酚酞后显无色的溶液 |
| C、能与金属Al反应放出H2的溶液 |
| D、c(H+)>c(OH-)的任意水溶液 |
查看答案和解析>>
科目: 来源: 题型:
| 灼烧 |
| 沸水 |
| 浸泡 |
| 过滤 |
| H+ |
| H2O2 |
| CCl4 |
| 蒸馏 |
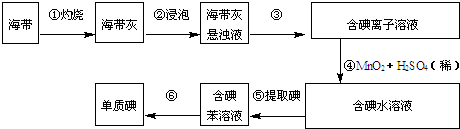
| A、实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌 |
| B、含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应 |
| C、在碘水中加入几滴淀粉溶液,溶液变蓝色 |
| D、碘水加入CCl4得到I2的CCl4溶液,该操作为“萃取” |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、在原电池中,电子流出的一极是负极,该电极得电子,被还原 |
| B、在燃料电池的负极发生反应的通常是可燃性气体 |
| C、电池内部填有NH4Cl等化学物质,将废电池中的黑色糊状物当做化肥用 |
| D、构成原电池的正极和负极必须是两种不同的金属 |
查看答案和解析>>
科目: 来源: 题型:
 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( ) | A、①②③ | B、③④⑤ |
| C、④⑤⑥ | D、②③④ |
查看答案和解析>>
科目: 来源: 题型:
| A、充电电池的化学反应原理是氧化还原反应 |
| B、充电电池的充电放电次数没有限制 |
| C、充电电池又称二次电池,充电时是使放电时的氧化还原反应逆向进行 |
| D、充电电池在充电时是将电能转变成化学能 |
查看答案和解析>>
科目: 来源: 题型:
| A、0.8mol?L-1 |
| B、1.0mol?L-1 |
| C、1.2mol?L-1 |
| D、2.0mol?L-1 |
查看答案和解析>>
科目: 来源: 题型:
 氮元素可以形成多种氢化物,如NH3、N2H4等.
氮元素可以形成多种氢化物,如NH3、N2H4等.| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
c(N
| ||
| c(NH3?H2O)?c(H +) |
查看答案和解析>>
科目: 来源: 题型:
 工业上将煤气化过程中生成的CO和H2在一定条件下反应制得甲醇,反应的方程式为:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题:
工业上将煤气化过程中生成的CO和H2在一定条件下反应制得甲醇,反应的方程式为:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.H分子中含有1个-CH3,苯环上只有一个取代基.又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).试回答下列问题.
肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.H分子中含有1个-CH3,苯环上只有一个取代基.又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).试回答下列问题.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com