
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

 通式表示(其中X、Y均不为氢),现有以下四种物质既符合上述通式又能发生银镜反应,其中在核磁共振氢谱图上能产生4个吸收峰的是
通式表示(其中X、Y均不为氢),现有以下四种物质既符合上述通式又能发生银镜反应,其中在核磁共振氢谱图上能产生4个吸收峰的是
 它可通过不同的反应分别得到下列物质:
它可通过不同的反应分别得到下列物质:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、①② | B、②③ | C、③④ | D、①④ |
查看答案和解析>>
科目: 来源: 题型:
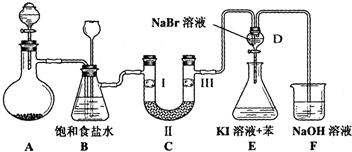
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com