
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
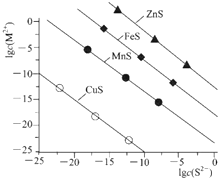 25℃时,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示.下列说法正确的是( )
25℃时,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示.下列说法正确的是( )| A、Ksp(CuS)约为l×10-20 |
| B、向Cu2+浓度为10-5mol?L-1废水中加入ZnS粉末,会有CuS沉淀析出 |
| C、向l00mL浓度均为10-5mol?L-1 Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol?L-1 Na2S溶液,Zn2+先沉淀 |
| D、Na2S溶液中:2c(S2-)+2c(HS-)+2c(H2S)=c(Na+) |
查看答案和解析>>
科目: 来源: 题型:
| A、氧化钠和过氧化钠含有相同的元素,与水反应的产物也相同 |
| B、CO2与SiO2的组成相同,两者的化学性质也相同 |
| C、铁和铜都属于金属,久置在潮湿的空气中均生成金属氧化物 |
| D、H2O2和Na2O2都有强氧化性,两者均能使品红溶液褪色 |
查看答案和解析>>
科目: 来源: 题型:
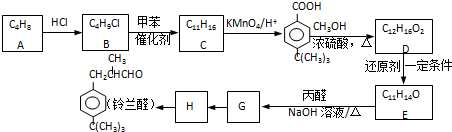
| NaOH溶液 |
| △ |
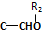
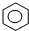
| 催化剂 |
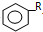 +HCl
+HCl查看答案和解析>>
科目: 来源: 题型:
| 选项 | W | X | Y | Z |  |
| A | S | SO2 | SO3 | H2SO4 | |
| B | Na | Na2O2 | NaOH | NaCl | |
| C | Fe | FeCl3 | Fe(OH)2 | FeCl2 | |
| D | Al | AlCl3 | NaAlO2 | Al2(SO4)3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目: 来源: 题型:
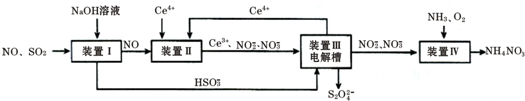
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目: 来源: 题型:

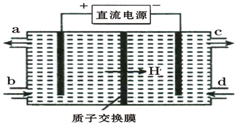
| A、该装置中铜为阳极 |
| B、当铜片的质量变化了12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
| C、该装置中b极的电极反应式是:H2+2OH--2e-═2H2O |
| D、该装置中a极为正极,发生氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com