
科目: 来源: 题型:
 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
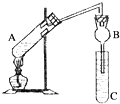 如图所示一套实验装置来制取乙酸乙酯,A中盛有乙醇、浓硫酸和醋酸的混合液,C中盛有饱和碳酸钠溶液.
如图所示一套实验装置来制取乙酸乙酯,A中盛有乙醇、浓硫酸和醋酸的混合液,C中盛有饱和碳酸钠溶液.| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 117.9 | 77.1 |
查看答案和解析>>
科目: 来源: 题型:
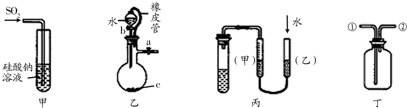
| A、甲装置:可用来证明硫的非金属性比硅强 |
| B、乙装置:橡皮管的作用是能使水顺利流下 |
| C、丙装置:用图示的方法能检查此装置的气密性 |
| D、丁装置:可在瓶中先装满水,气体由②口入,收集NO气体 |
查看答案和解析>>
科目: 来源: 题型:
| C2H5ONa |
| 钠 | 苯 | 甲苯 | 对二甲苯 | 四氯化碳 | |
| 密度(g/cm3) | 0.97 | 0.88 | 0.87 | 0.86 | 1.60 |
| 熔点(℃) | 97.8 | 5.5 | -95 | 13.3 | -22.8 |
| 沸点(℃) | 881.4 | 80 | 111 | 138.4 | 76.8 |
| 无水硫酸钠 |
| 操作X |
| 水浴蒸馏 |
| 减压蒸馏 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、氢氧化钠用于治疗胃溃疡病人的胃酸过多症 |
| B、金属钠具有强的还原性,可利用钠和TiCl4溶液反应制取金属Ti |
| C、糖类、油脂、蛋白质在一定条件下均可以水解 |
| D、在常温下,浓硫酸、浓硝酸能用铁罐储运 |
查看答案和解析>>
科目: 来源: 题型:
| A、125g CuSO4?5H2O晶体中含有Cu2+离子数小于0.5NA |
| B、7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA |
| C、由S4、S6、S8组成的硫蒸气6.4 g,其中所含硫原子数一定为0.2NA |
| D、3.6 gC与3.36LO2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |
查看答案和解析>>
科目: 来源: 题型:
| A、常温常压下,48gO3含有的氧为3NA |
| B、标准状况下,22.4 L水含有的水分子数为NA |
| C、常温常压下,11.2 L氧气所含的原子数小于NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com