
科目: 来源: 题型:
| A、同温度下,CuS的溶解度大于FeS的溶解度 |
| B、同温度下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)变小 |
| C、向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,最先出现的沉淀是FeS |
| D、除去工业废水中的Cu2+,可以选用FeS作沉淀剂 |
查看答案和解析>>
科目: 来源: 题型:
| A、在一定温度下的饱和AgCl水溶液中,Ag+与Cl-的浓度乘积是一个常数 |
| B、已知AgCl的Ksp=1.8×10-10 mol2?L-2,则在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-),且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2?L-2 |
| C、Ksp数值越大的难溶电解质在水中的溶解能力越强 |
| D、难溶电解质的溶解程度很小,故外界条件改变,对它的溶解程度没有影响 |
查看答案和解析>>
科目: 来源: 题型:
| A、c(Ag+)≠c(Cl-),c(Ag+)?c(Cl-)≠Ksp(AgCl) |
| B、c(Ag+)≠c(Cl-),c(Ag+)?c(Cl-)=Ksp(AgCl) |
| C、c(Ag+)=c(Cl-),c(Ag+)?c(Cl-)≠Ksp(AgCl) |
| D、c(Ag+)=c(Cl-),c(Ag+)?c(Cl-)=Ksp(AgCl) |
查看答案和解析>>
科目: 来源: 题型:
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A、相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
| B、向碳酸钠溶液中滴加少量氯水的离子方程式为:CO32-+Cl2+H2O═HCO3-+Cl-+HClO |
| C、向0.1mol?L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=5 |
| D、向浓度均为0.001 mol?L-1的KCl和K2CrO4混合液中滴加0.001 mol?L-1AgNO3溶液,CrO42-先形成沉淀 |
查看答案和解析>>
科目: 来源: 题型:
| A、在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| B、相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol?L-1盐酸、③0.1 mol?L-1氯化镁溶液、④0.1 mol?L-1硝酸银溶液中,Ag+浓度:①>④=②>③ |
| C、向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-=Ag2S↓+2Cl- |
| D、25℃时,在Mg(OH)2悬浊液中加入少量的NH4Cl固体后,c(Mg2+)减小 |
查看答案和解析>>
科目: 来源: 题型:
| 实验编号 | HA物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、0.1 mol?L-1 NaHSO4溶液中:[Na+]>[SO42-]>[H+]>[OH-] |
| B、0.1 mol?L-1Na2S溶液中:2[Na+]=[S2-]+[HS-]+[H2S] |
| C、0.1 mol?L-1 NaHCO3溶液中:[Na+]+[H+]=[HCO3-]+2[CO32-]+[OH-] |
| D、等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:[Na+]=[CH3COO-]>[H+]=[OH-] |
查看答案和解析>>
科目: 来源: 题型:
| A、四种溶液中c(HA-)浓度大小:③>①>②>④ |
| B、溶液①中粒子浓度大小顺序是:c(H2A)>c(H+)>c(HA-)>c(A2-)>c(OH-) |
| C、溶液②中有关离子浓度关系:c(HA-)+2c(A2-)+c(H2A)=c(Na+) |
| D、溶液③中有关离子浓度关系:c(HA-)+c(A2-)+c(OH-)=c(Na+)+c(H+) |
查看答案和解析>>
科目: 来源: 题型:
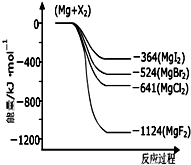 (1)写出实验室用二氧化锰和浓盐酸反应制取氯气的离子方程式
(1)写出实验室用二氧化锰和浓盐酸反应制取氯气的离子方程式查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com