
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
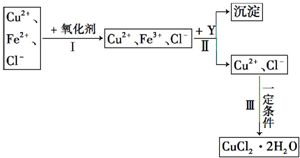 CuCl2溶液中含有少量杂质FeCl2,为制备纯净的CuCl2?2H2O晶体,拟定实验步骤如图所示:请回答下列问题:
CuCl2溶液中含有少量杂质FeCl2,为制备纯净的CuCl2?2H2O晶体,拟定实验步骤如图所示:请回答下列问题:查看答案和解析>>
科目: 来源: 题型:
A、14+
| ||||
B、14+
| ||||
C、
| ||||
D、
|
查看答案和解析>>
科目: 来源: 题型:
| A、由水电离的c(H+):①=②>③=④ |
| B、将①、④两种溶液混合后,若pH=7,则消耗溶液的体积:①>④ |
| C、①②的导电性不同,③④的导电性也不同 |
| D、向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>②>① |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ①KMnO4、OH- | ||
|
| HBr |
| 过氧化物 |
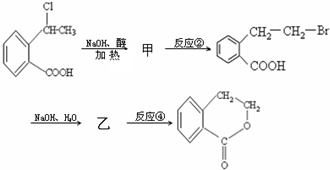
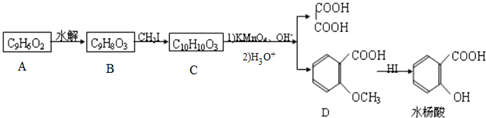
查看答案和解析>>
科目: 来源: 题型:
| 实验序号 | 0.1032mol/L HCI体积体积/mL | 待测NaOH溶液体积/mL |
| 1 | 27.83 | 25.00 |
| 2 | 26.53 | 25.00 |
| 3 | 27.85 | 25.00 |
查看答案和解析>>
科目: 来源: 题型:
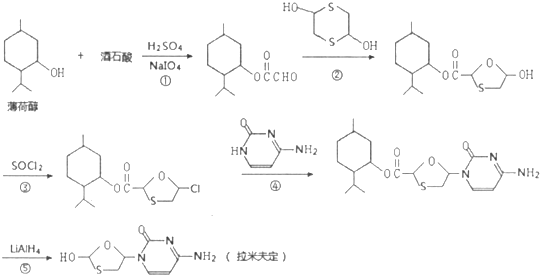
| HIO4 |
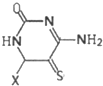 (其中X表示剩余的部分)
(其中X表示剩余的部分)查看答案和解析>>
科目: 来源: 题型:
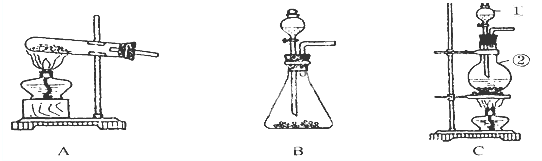
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com