
科目: 来源: 题型:
| A、11.76g |
| B、14 g |
| C、25.2g |
| D、28g |
查看答案和解析>>
科目: 来源: 题型:
| A、1000mL,212g |
| B、950mL,100.7g |
| C、任意规格,572g |
| D、500mL,286g |
查看答案和解析>>
科目: 来源: 题型:
 蒸馏是提纯或分离
蒸馏是提纯或分离| 2 |
| 3 |
| 1 |
| 3 |
查看答案和解析>>
科目: 来源: 题型:
| A、某溶液中加入盐酸产生气体,则其中一定含有CO32- |
| B、用焰色反应检验钠元素的存在 |
| C、用氢氧化钠溶液和湿润的红色石蕊试纸检验NH4+ |
| D、用盐酸和氯化钡溶液检验 SO42- |
查看答案和解析>>
科目: 来源: 题型:
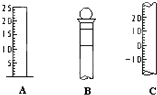 (1)对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等.下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等.下列各组混和物的分离或提纯应采用什么方法?(填序号)查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
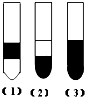 在盛有碘水的三支试管中,分别加入苯、四氯化碳和酒精,充分振荡后静置,出现如图所示的现象,正确的结论是( )
在盛有碘水的三支试管中,分别加入苯、四氯化碳和酒精,充分振荡后静置,出现如图所示的现象,正确的结论是( )| A、(1)中加入的是CCl4(2)加入的是苯(3)加入的是酒精 |
| B、(1)中加入的是酒精(2)加入的是CCl4(3)加入的是苯 |
| C、(1)中加入的是苯(2)加入的是酒精(3)加入的是CCl |
| D、(1)中加入的是苯(2)加入的是CCl4(3)加入的是酒精 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com