
科目: 来源: 题型:
| c(X)?c2(Y) |
| c2(Z)?c2(W) |
| A、该反应可表示为X(g)+2Y(g)?2Z(g)+2W(g) |
| B、减小X浓度,该反应速率一定减小,平衡向逆反应方向移动 |
| C、增大反应容器的压强,平衡常数K减小 |
| D、升高温度,W(g)体积分数增加,则正反应是放热反应 |
查看答案和解析>>
科目: 来源: 题型:
| A、OH-Ba2+NO3-K+ |
| B、Na+ SO42- Cu2+ Cl- |
| C、HCO3- Cl- Na+ Ba2+ |
| D、Fe3+ Al3+ I- NO3- |
查看答案和解析>>
科目: 来源: 题型:
| A、Na+、NH4+、Br-、Cl- |
| B、K+、Na+、SO42 -、SiO32 - |
| C、Na+、HCO3-、SO32 -、CH3COO- |
| D、H+、Fe3+、NO3-、SO32 - |
查看答案和解析>>
科目: 来源: 题型:
| A、生成n mol的A2,同时生成 n mol的AB |
| B、密闭容器内总压强不随时间变化 |
| C、生成2n mol的AB,同时生成n mol的B2 |
| D、生成n mol的A2,同时生成的n molB2 |
查看答案和解析>>
科目: 来源: 题型:
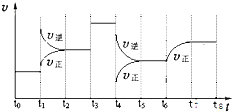 T℃时,在某容积恒为2L密闭容器中充入2molN2、4molH2,在催化剂辅助下发生反应:N2(g)+3H2(g)?2NH3(g)△H=-92.0kJ/mol.t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如图所示.
T℃时,在某容积恒为2L密闭容器中充入2molN2、4molH2,在催化剂辅助下发生反应:N2(g)+3H2(g)?2NH3(g)△H=-92.0kJ/mol.t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如图所示.查看答案和解析>>
科目: 来源: 题型:
| A、pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | ||
B、
| ||
| C、由水电离的c(H+)=1×10-14mol?L-1的溶液中:Ca2+、K+、Cl-、HCO3- | ||
| D、c(Fe3+)=0.1mol?L-1的溶液中:K+、ClO-、SO42-、SCN- |
查看答案和解析>>
科目: 来源: 题型:
| A、Ag+、Ba2+、Cl- |
| B、Na+、HCO3-、OH- |
| C、NH4+、SO42-、NO3- |
| D、K+、OH-、Fe3+ |
查看答案和解析>>
科目: 来源: 题型:
| A、Mg2+ |
| B、Fe3+ |
| C、Cl- |
| D、Ba2+ |
查看答案和解析>>
科目: 来源: 题型:
| A、分类回收垃圾 |
| B、举行地球一小时熄灯活动 |
| C、大力发展火力发电厂 |
| D、大规模开展植树造林、退耕还林还草等工作 |
查看答案和解析>>
科目: 来源: 题型:
| c(OH-) |
| c(H+) |
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com