
科目: 来源: 题型:
| NaCl |
| NH4Cl |
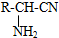 ,R-CN
,R-CN| H+ |
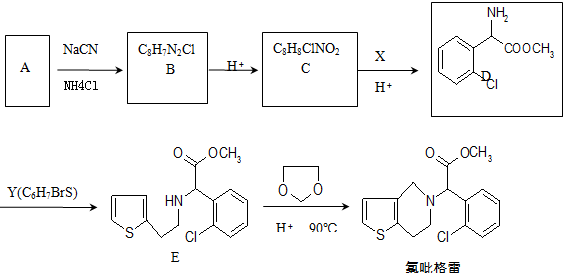
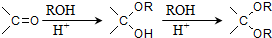 ,写出由乙烯、甲醇为有机原料制备化合物
,写出由乙烯、甲醇为有机原料制备化合物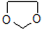 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH3CH2OH| 浓硫酸 |
| 170℃ |
| Br2 |
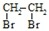
查看答案和解析>>
科目: 来源: 题型:
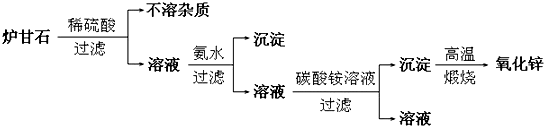
| 离子 | Fe3+ | Cu2+ | Zn2+ |
| 完全沉淀时的pH | 3.2 | 6.7 | 8.0 |
查看答案和解析>>
科目: 来源: 题型:

 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是查看答案和解析>>
科目: 来源: 题型:
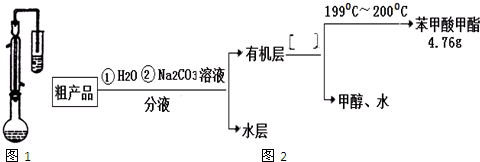
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
查看答案和解析>>
科目: 来源: 题型:
| PCl3 |
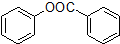 )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).| O2 |
| 催化剂 |
| CH3CH2OH |
| 浓H2SO4 |
查看答案和解析>>
科目: 来源: 题型:
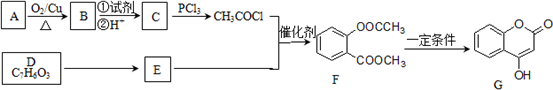
 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:
| A、1mol双酚A最多可与2mol Br2反应 |
| B、G物质是乙醛的同系物 |
| C、E物质的名称是1-溴丙烷 |
D、反应③的化学方程式是 |
查看答案和解析>>
科目: 来源: 题型:
| 药品名称 | 熔点/℃ | 沸点(℃) | 密度 g/cm3 | 溶解性 |
| 正丁醇 | -89.5 | 117.7 | 0.8098 | 微溶于水、溶于浓硫酸 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.2760 | 不溶于水和浓硫酸 |
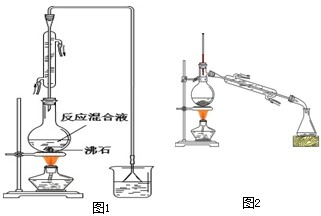
查看答案和解析>>
科目: 来源: 题型:
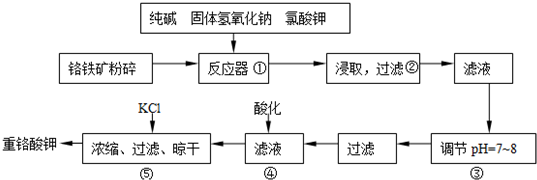
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
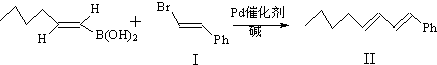
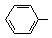 ):
):
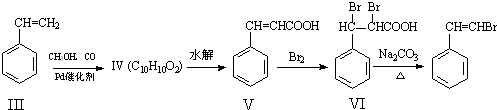
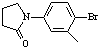 )与化合物(
)与化合物(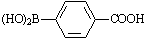 )能发生偶联反应生成一种抗抑郁药物,写出该抗抑郁药物的结构简式
)能发生偶联反应生成一种抗抑郁药物,写出该抗抑郁药物的结构简式查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com