
科目: 来源: 题型:
 正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下: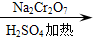 CH3CH2CH2CHO
CH3CH2CH2CHO| 沸点/℃ | 密度/(g?cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目: 来源: 题型:
| A、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |
| B、常温下,1 mol?L-1的CH3COOH溶液与1 mol?L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、将AlCl3溶液加热蒸干并灼烧后剩余固体为Al2O3 |
| D、常温下,某溶液中由水电离出的c(H+)=10-5 mol?L-1,则此溶液可能是盐酸 |
查看答案和解析>>
科目: 来源: 题型:
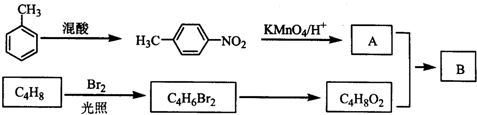
查看答案和解析>>
科目: 来源: 题型:
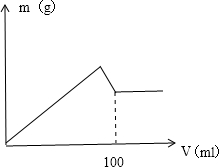 有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.
有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.查看答案和解析>>
科目: 来源: 题型:
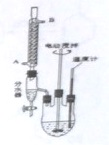 邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:
邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:查看答案和解析>>
科目: 来源: 题型:
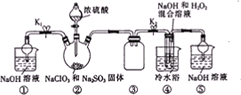 已知亚铝酸钠(NaClO2)为白色粉末,易溶于水,NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2
已知亚铝酸钠(NaClO2)为白色粉末,易溶于水,NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、3种 | B、4种 | C、5种 | D、6种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com