
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、元素的非金属性:X>Y>Z |
| B、原子序数:X>Y>Z |
| C、气态氢化物的稳定性:XH3>YH3>ZH3 |
| D、气态氢化物的还原性:XH3<YH3<ZH3 |
查看答案和解析>>
科目: 来源: 题型:
 镁是海水中含量较多的金属,镁、镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛.
镁是海水中含量较多的金属,镁、镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛.| n(NH3) |
| n(CO2) |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、AgCl沉淀的生成和溶解在达到平衡时就不再进行 |
| B、AgCl不溶于水,溶液中没有Cl-和Ag+ |
| C、升高温度,AgCl的溶解度增大,Ksp增大 |
| D、向AgCl饱和溶液中加入NaCl固体,AgCl的溶解度和Ksp都不变 |
查看答案和解析>>
科目: 来源: 题型:
| A、用铂丝蘸取某盐溶液进行焰色反应,火焰呈黄色,说明该盐溶液含钠元素,一定不含钾元素 |
| B、配制100 mL 1 mol/L NaCl溶液,定容时俯视刻度线,则所配溶液浓度偏小 |
| C、只用胶头滴管和试管,不用其他试剂无法区别稀盐酸和K2CO3稀溶液 |
| D、纳米材料微粒直径一般从几纳米到几十纳米,将纳米材料分散到溶剂中得到的分散系,用可见光束照射具有丁达尔效应 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、反应速率v(C)=1mol?L-1?s-1 |
| B、C的平衡浓度为4 mol?L-1 |
| C、A的转化率为25% |
| D、B的平衡浓度为1.5 mol?L-1 |
查看答案和解析>>
科目: 来源: 题型:
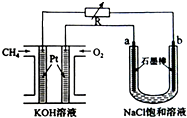 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组用甲烷燃料电池作为电源,进行饱和氯化钠溶液电解实验,如图所示:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组用甲烷燃料电池作为电源,进行饱和氯化钠溶液电解实验,如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com