
科目: 来源: 题型:
| 一定条件 |
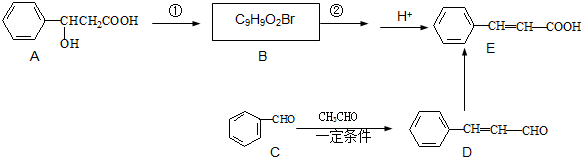
 是有机物A的同分异构体,下列说法错误的是
是有机物A的同分异构体,下列说法错误的是查看答案和解析>>
科目: 来源: 题型:

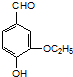
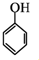 和乙酸酐为原料制备
和乙酸酐为原料制备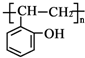 的合成路
的合成路| NaOH溶液 |
| △ |
| CH3COOH |
| 浓硫酸,△ |
查看答案和解析>>
科目: 来源: 题型:
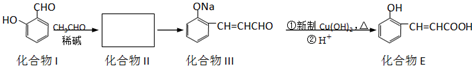
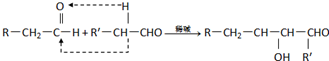
查看答案和解析>>
科目: 来源: 题型:

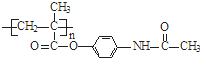
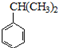 可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色;反应②为加成反应
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色;反应②为加成反应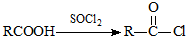
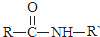
| NaOH溶液 |
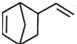 属于芳香烃的同分异构体的同系物制备
属于芳香烃的同分异构体的同系物制备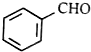 的合成路线,
的合成路线,| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目: 来源: 题型:
| V(NaOH) | V(KHP)平均 |
| 20.00mL | 18.00mL |
| V(稀释后的醋) | V(NaOH)平均 |
| 18.00mL | 20.00mL |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| 金属离子 | 开始沉演的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 9.6 |
| Co2+ | 5.8 | 9.4 |
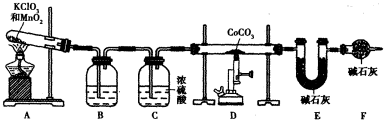
| x |
| y |
查看答案和解析>>
科目: 来源: 题型:
| 序号 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 |  选用滴定管 选用滴定管 |
| A | 碱 | 酸 | 石芯 | (乙) |
| B | 酸 | 碱 | 酚酞 | (甲) |
| C | 碱 | 酸 | 甲基橙 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
| 实验 编号 | 待测氢氧化钠溶液体积(mL) | 滴定开始读数(mL) | 滴定结束读数(mL) | 消耗盐酸体积(mL) |
| ① | 25.00 | 0.02 | 26.40 | |
| ② | 25.00 | 0.04 | 25.81 | |
| ③ | 25.00 | 0.03 | 25.78 | |
| ④ | 25.00 | 0.20 | 25.96 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
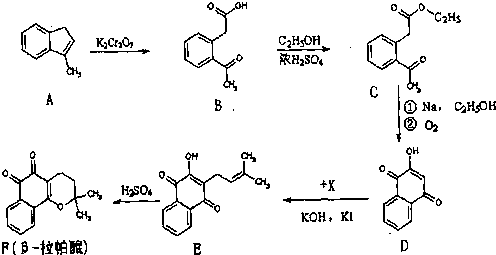
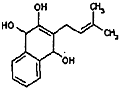 ,写出此有机物分子中含有的官能团名称:
,写出此有机物分子中含有的官能团名称: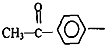 结构且能水解的所有同分异构体的结构简式:
结构且能水解的所有同分异构体的结构简式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com