
科目: 来源: 题型:
| A、甲苯和乙苯 | B、乙烯和丙烯 |
| C、乙烷和乙烯 | D、乙烯和苯 |
查看答案和解析>>
科目: 来源: 题型:
| A、待检液逐滴加入NaOH溶液,有白色胶状沉淀产生后来沉淀逐渐消失,则原溶液中可能含有Al3+ |
| B、待检液中先加入KSCN溶液,无明显现象,再加入氯水溶液显血红色,则待检液中一定含有Fe2+ |
| C、将某化合物进行焰色实验,透过蓝色钴玻璃观察,焰色为紫色,证明含K+ |
| D、向某物质中滴加盐酸后,有能使澄清石灰水变浑浊的无色无味气体产生,证明含CO32- |
查看答案和解析>>
科目: 来源: 题型:
| ||
| A、11.43 |
| B、22.85 |
| C、80.01 |
| D、160.02 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、某酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a≤b-1 |
| B、在滴酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的c (NH4+)=c(Cl-) |
| C、常温下,某硫酸溶液的pH=3,升高其温度,溶液pH增大 |
| D、相同温度、相同体积、相同物质的量浓度的KI和KF溶液中,离子总数前者大于后者 |
查看答案和解析>>
科目: 来源: 题型:
| 催化剂 |
| △ |
 | p1(Mpa) | p2(Mpa) |
| 400℃ | 99.6 | 99.7 |
| 500℃ | 96.9 | 97.8 |
A、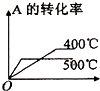 |
B、 |
C、 |
D、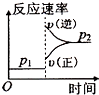 |
查看答案和解析>>
科目: 来源: 题型:
 向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol?L-1 HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol?L-1 HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )| A、a曲线表示的离子方程式为:AlO2-+H++H2O═Al(OH)3↓ |
| B、b和c曲线表示的离子反应是相同的 |
| C、M点时,溶液中沉淀的质量为3.9g |
| D、原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
查看答案和解析>>
科目: 来源: 题型:
 纳米级Cu2O由于具有优良的催化性能而受到科学研究的不断关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到科学研究的不断关注,下表为制取Cu2O的三种方法:| 方法Ⅰ | 用炭粉在高温条件下还原CuO | ||||
| 方法Ⅱ | 电解法,反应为2Cu+H2O
| ||||
| 方法Ⅲ | 用肼(N2H4)还原新制的Cu (OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com