
科目: 来源: 题型:
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.0O | 4.10 | 24.00 |
查看答案和解析>>
科目: 来源: 题型:
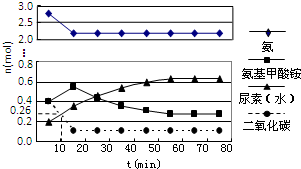 尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步:
尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 一定条件 |



查看答案和解析>>
科目: 来源: 题型:
 所示.试回答下列问题:
所示.试回答下列问题:
查看答案和解析>>
科目: 来源: 题型:
 如图所示,在一盛有蒸馏水的烧杯中有一悬浮的小球,当向烧杯中加入(或通入)下列物质后,小球沉到水底的是( )
如图所示,在一盛有蒸馏水的烧杯中有一悬浮的小球,当向烧杯中加入(或通入)下列物质后,小球沉到水底的是( )| A、HCl |
| B、NH3 |
| C、浓H2SO4 |
| D、浓HNO3 |
查看答案和解析>>
科目: 来源: 题型:

| A、装置A中药品应为浓硫酸 |
| B、在B-C之间应增添盛有饱和NaHCO3溶液的洗气装置,以除去氯化氢气体 |
| C、为了测得C中生成的沉淀质量,需经过过滤、洗涤、干燥、称量等操作 |
| D、只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数 |
查看答案和解析>>
科目: 来源: 题型:
| A、制阿司匹林时用水洗涤产品,而在制摩尔盐时用酒精洗涤产品 |
| B、纸层析法通常把不与水混溶的有机溶剂作为固定相 |
| C、中和滴定实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,必须干燥或润洗后方可使用 |
| D、减压过滤装置中,布氏漏斗的颈口斜面应与吸滤瓶的支管口相对,以便于吸滤 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
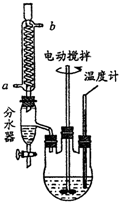 草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC-COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:
草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC-COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com