
科目: 来源: 题型:
| A、HCO3-在水溶液中只电离,不水解 |
| B、硝酸钠溶液水解之后呈中性 |
| C、可溶性的铝盐都能发生水解反应 |
| D、可溶性的钾盐都不能发生水解反应 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
查看答案和解析>>
科目: 来源: 题型:
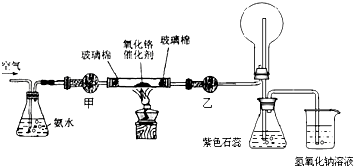
查看答案和解析>>
科目: 来源: 题型:
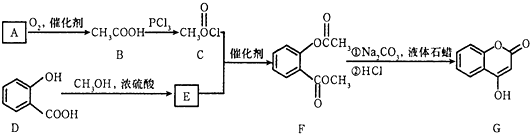
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA |
| B、标况下,22.4L SO3含有NA个SO3分子 |
| C、78g Na2O2与足量水充分反应时电子转移数为2NA |
| D、4℃、101.3kPa时,54mL H2O中含有的分子数为3NA |
查看答案和解析>>
科目: 来源: 题型:
 元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,
元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com