
科目: 来源: 题型:
| A、化合物:干冰、冰水混合物、烧碱、小苏打 |
| B、非电解质:乙醇、四氯化碳、氯气、葡萄糖 |
| C、胶体:泥水、豆浆、有色玻璃、云、雾 |
| D、混合物:铝热剂、纯净矿泉水、水玻璃、漂白粉 |
查看答案和解析>>
科目: 来源: 题型:
| A、用激光笔光束鉴别氯化铁溶液和氢氧化铁胶体 |
| B、用KSCN溶液鉴别Fe3+和Fe2+ |
| C、用氨水鉴别Al3+和Mg2+ |
| D、用焰色反应鉴别碳酸钠溶液和碳酸钾溶液 |
查看答案和解析>>
科目: 来源: 题型:
| 编号 | 物质 | 试剂名称 |
| ① | 除杂质:NaHCO3溶液(Na2CO3) | |
| ② | 除杂质:SiO2(CaCO3) | |
| ③ | 除杂质:FeCl2溶液(FeCl3) | |
| ④ | 鉴别:Na2CO3 Na2SiO3溶液 | |
| ⑤ | 鉴别:(NH4)2SO4 NH4C1Na2SO4溶液 |
查看答案和解析>>
科目: 来源: 题型:
 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )| A、①②③ | B、②④⑤ |
| C、①②④⑥ | D、②③⑥ |
查看答案和解析>>
科目: 来源: 题型:
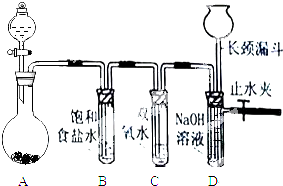 Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证该结论,学生设计了如图所示的实验装置进行实验(夹持装置略去).圆底烧瓶A中的反应方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,请回答下列问题.
Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证该结论,学生设计了如图所示的实验装置进行实验(夹持装置略去).圆底烧瓶A中的反应方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,请回答下列问题.查看答案和解析>>
科目: 来源: 题型:
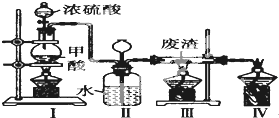
| A、Ⅲ、Ⅰ、Ⅳ |
| B、Ⅰ、Ⅲ、Ⅳ |
| C、Ⅲ、Ⅳ、Ⅰ |
| D、I、Ⅳ、Ⅲ |
查看答案和解析>>
科目: 来源: 题型:
| A、1:5 | B、5:1 |
| C、1:1 | D、3:5 |
查看答案和解析>>
科目: 来源: 题型:
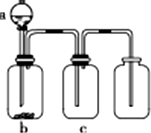 用如图所示装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂,且尾气处理装置略),其中可行的是( )
用如图所示装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂,且尾气处理装置略),其中可行的是( )| 气体 | a | b | c | |
| A | NO2 | 浓硝酸 | 铜片 | 浓硫酸 |
| B | SO2 | 浓硫酸 | Cu | 酸性KMnO4溶液 |
| C | CO2 | 稀硫酸 | CaCO3 | 浓硫酸 |
| D | NH3 | 浓氨水 | 生石灰 | 浓硫酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 某学生用0.1000mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如
某学生用0.1000mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com