
科目: 来源: 题型:
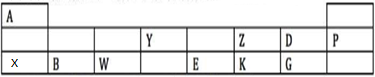
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
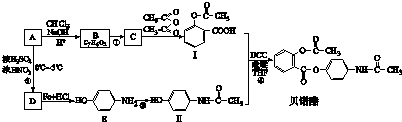
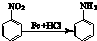
查看答案和解析>>
科目: 来源: 题型:

| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
查看答案和解析>>
科目: 来源: 题型:
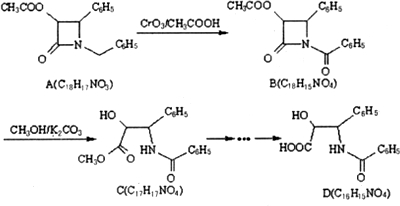
| K2CO3 |
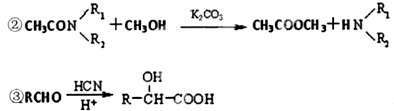
| PCl3 |

查看答案和解析>>
科目: 来源: 题型:
 使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.
使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.滴定次数 实验数据/mL | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.80 | 15.00 | 15.02 | 14.98 |
查看答案和解析>>
科目: 来源: 题型:
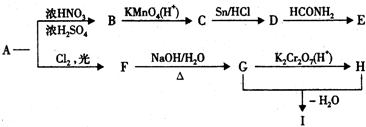
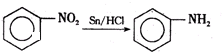

 ,物质E含2个六元环.
,物质E含2个六元环.查看答案和解析>>
科目: 来源: 题型:
| A、SO2能使品红溶液褪色,是因为SO2具有漂白性 |
| B、SO2在空气中极易被氧化为SO3 |
| C、SO2通入Na2SO3或NaHCO3溶液中均能发生反应 |
| D、SO2是形成酸雨的大气污染物之一,主要来自于化石燃料的燃烧和工厂排放的废气 |
查看答案和解析>>
科目: 来源: 题型:
 如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成.据此判断下列说法中不正确的是( )
如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成.据此判断下列说法中不正确的是( )| A、上述反应是置换反应 |
| B、上述反应说明钠比铜活泼 |
| C、上述反应证明钠可以从CuSO4溶液中置换出铜 |
| D、加热且无水条件下,Na可以与CuSO4反应并生成Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com