
科目: 来源: 题型:
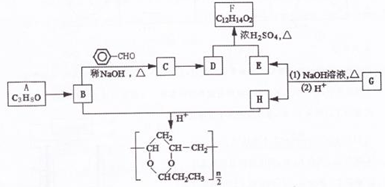
| 稀NaOH |
| △ |
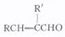 +H2O(R、R′表示烃基或氢)
+H2O(R、R′表示烃基或氢)
查看答案和解析>>
科目: 来源: 题型:
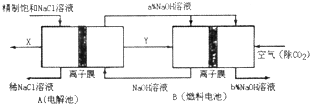
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、1:1 | B、2:1 |
| C、1:2 | D、任意比 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、原子半径:Na<Mg<Al |
| B、热稳定性:HCl>H2S>PH3 |
| C、酸性强弱:H4SiO4<H2CO3<CH3COOH |
| D、熔点:金刚石>食盐>干冰 |
查看答案和解析>>
科目: 来源: 题型:
 现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.| A原子的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol, |
| D原子核外所有P轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
查看答案和解析>>
科目: 来源: 题型:
| A、非金属性:A>C |
| B、原子半径:B<C<D |
| C、最高价氧化物对应水化物的酸性:D<C |
| D、单质B常温下能溶于浓硝酸 |
查看答案和解析>>
科目: 来源: 题型:

| A、T所在的周期数等于其主族序数 |
| B、含T元素的盐,其水溶液一定显酸性 |
| C、Z的含氧酸一定为强酸 |
| D、Q,R,J三元素中J的电负性最大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com