
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
 为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g 以如图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g 以如图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)查看答案和解析>>
科目: 来源: 题型:
| △ |

查看答案和解析>>
科目: 来源: 题型:
| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(mL) | 15.40 | 12.90 | 13.10 | 13.00 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
 某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:
某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:查看答案和解析>>
科目: 来源: 题型:
 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件及部分产物未列出).
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件及部分产物未列出).查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
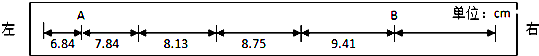
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com