
科目: 来源: 题型:
| 步骤 | 加入的试剂 | 作用 |
| 1 | ||
| 2 | ||
| 3 | ||
| … | ||
查看答案和解析>>
科目: 来源: 题型:
| A、用氢氧化钠溶液可以鉴别NH4C1和NH4NO3两种物质 |
| B、用焰色反应可以鉴别出NaCl和K2SO4两种无色溶液 |
| C、用盐酸可以鉴别NaHCO3、Na2CO3两种白色固体 |
| D、用丁达尔效应可以鉴别氢氧化铝胶体和氯化铝溶液 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| T/(K) | 298 | 398 | 498 | … |
| K | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
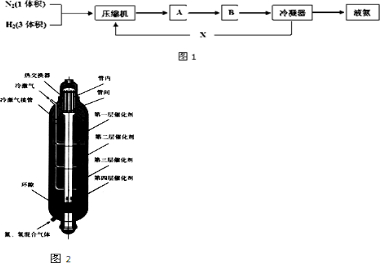
 (1)如图1所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气.过一段时间后可观察到
(1)如图1所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气.过一段时间后可观察到| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
科目: 来源: 题型:
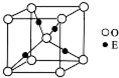 已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基
已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基查看答案和解析>>
科目: 来源: 题型:
| A、用碱式滴定管量取0.10 mol?L-1的Na2CO3溶液22.10 mL |
| B、配制一定浓度的氢氧化钠溶液时,将氢氧化钠固体放在纸片上称量 |
| C、用广范pH试纸测某HCl溶液pH=3.6 |
| D、用玻璃棒蘸取HCl溶液滴到湿润的pH试纸上,测其pH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com