
科目: 来源: 题型:
 卤代烃里的卤原子易与活泼金属阳离子结合,发生下列反应:
卤代烃里的卤原子易与活泼金属阳离子结合,发生下列反应:| 乙醇 |
| 乙醇溶液 |
查看答案和解析>>
科目: 来源: 题型:
| A、2g | B、1.6g |
| C、1g | D、1.8g |
查看答案和解析>>
科目: 来源: 题型:
| A、还原剂 |
| B、氧化剂 |
| C、既是还原剂又是氧化剂 |
| D、既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目: 来源: 题型:
| A、2.4 g |
| B、3.2 g |
| C、6.4 g |
| D、9.6 g |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 化学键 | C-C | C-H | H-H | C-O | C O | H-O |
| 能量/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 3 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目: 来源: 题型:
| A、只有③④ | B、均不合理 |
| C、只有⑤⑥ | D、只有①②⑥ |
查看答案和解析>>
科目: 来源: 题型:
 (1)工业酸性废水中含Cr2O72-离子会造成铬污染,排放前先将Cr2O72-还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气.结果溶液的PH值不断升高,溶液由酸性转变为碱性.Cr2O72-转化为毒性较低的Cr3+的离子方程式为:
(1)工业酸性废水中含Cr2O72-离子会造成铬污染,排放前先将Cr2O72-还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气.结果溶液的PH值不断升高,溶液由酸性转变为碱性.Cr2O72-转化为毒性较低的Cr3+的离子方程式为:查看答案和解析>>
科目: 来源: 题型:
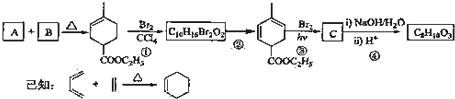
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com